
| 实验编号 | 选用金属(质量形状相同) | 盐酸浓度(相同体积) | 产生氢气的体积/mL | |||||
| 0 | t1 | t2 | t3 | t4 | t5 | |||
| Ⅰ | 锌片 | 6% | 0 | 1 | 2 | 3 | 3 | 3 |
| Ⅱ | 锌片 | 3% | 0 | 0.6 | 1.2 | 1.8 | 2.4 | 3 |

分析 根据已有的金属与酸的反应以及反应的剧烈程度的影响因素进行分析解答即可.
解答 解:(1)锌与稀盐酸反应产生大量的气泡,锌与稀盐酸反应生成氯化锌和氢气,发生反应的化学方程式是Zn+2HCl═ZnCl2+H2↑;故填:大量气泡,Zn+2HCl═ZnCl2+H2↑;
(2)铁与盐酸反应生成的氯化亚铁的水溶液呈浅绿色,故填:浅绿;
(3)根据锌与盐酸反应速率大,而铁的反应速率小可以看出,锌的活动性强于铁,故填:>;
(4)有反应的现象可以看出,金属的活动性越强,与相同的盐酸反应越剧烈,故填:金属的活动性越强,与相同的盐酸反应越剧烈;
(5)根据横坐标为时间,纵坐标为气体的体积,可以画出图示为: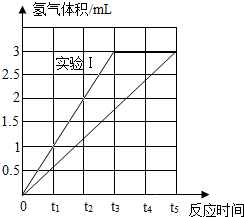
(6)相同条件下,盐酸的浓度越大,金属与盐酸反应越快,故填:快;
(7)金属与盐酸反应的剧烈程度可能温度有关,故填:温度.
点评 本题考查的是金属与酸反应的剧烈程度的影响因素的实验探究的知识,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 实验室里用氯酸钾制取氧气的装置如图所示,回答下列问题:
实验室里用氯酸钾制取氧气的装置如图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 双面使用纸张 | B. | 大量砍伐森林 | ||
| C. | 提倡使用一次性木筷 | D. | 尽量使用私家车等交通工具 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生白雾,放出大量的热 | |
| B. | 铁丝在氧气中燃烧火星四射,放出大量的热,生成黑色的固体 | |
| C. | 硫在空气中燃烧,产生明亮蓝紫色火焰,生成刺激性气味的二氧化硫 | |
| D. | 镁带在空气中燃烧,放出大量的热,生成黑色固体氧化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀有气体化学性质很不活泼,所以可制成多种电光源 | |
| B. | 火碱具有碱性,故可用于改良酸性土壤 | |
| C. | 一氧化碳具有还原性,故可用于治金工业 | |
| D. | 高锰酸钾受热分解生成氧气,故工业上常用此方法制取氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com