
| 温度(℃) | 0 | 20 | 25 | 60 |
| Ba(OH)2溶解度 | 1.67 | 3.89 | 5.60 | 20.94 |
| Ca(OH)2溶解度 | 0.189 | 0.173 | 0.148 | 0.121 |
分析 (1)根据流程图,根据反应的特点,完成对所涉及反应的分析与推断;
(2)根据两物质的溶解度与温度关系,分析加热对两物质在水中溶解的影响,判断进行加热的原因;
(3)根据此时的溶解度,判断充分溶解后的溶液是否为饱和溶液,计算溶液的质量分数;
(4)根据对题中所述绿色化学的理解,判断流程图中所涉及的变化中体现出绿色化学理念的反应.
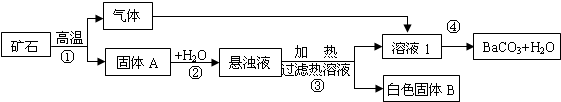
解答 解:(1)根据钡元素化合物的化学性质与钙元素化合物的化学性质相近的信息,可知矿石A高温下发生分解所产生的气体为二氧化碳;分解所得二氧化碳通入过滤所得氢氧化钡溶液即溶液1中,二氧化碳与氢氧化钡反应生成碳酸钡沉淀和水,化学方程式为:CO2+Ba(OH)2=BaCO3↓+H2O;
(2)对比所给出的氢氧化钙、氢氧化钡的溶解度表,会得到随温度升高氢氧化钙溶解度降低而氢氧化钡溶解度升高;温度越高氢氧化钡的溶解度越大,氢氧化钙的溶解度越小,因此在较高温度下过滤得到的氢氧化钡溶液中所含氢氧化钙杂质就越少;
(3)25℃时氢氧化钡的溶解度为5.60g,此时将10g氢氧化钡放入50g水中,充分搅拌,所得溶液为饱和溶液,其溶质的质量分数=$\frac{5.6g}{100g+5.6g}$×100%=5.3%;
(4)根据绿色化学的核心是利用化学原理来减少和消除工业生产对环境的影响,而流程中反应④消耗分解时所产生的二氧化碳,可减少向大气中的排放量,有效保护环境,体现出绿色化学的理念.
故答案为:(1)二氧化碳,CO2+Ba(OH)2=BaCO3↓+H2O;
(2)温度越高氢氧化钡的溶解度越大,氢氧化钙的溶解度越小,因此在较高温度下过滤得到的氢氧化钡溶液中所含氢氧化钙杂质就越少;
(3)5.3%;
(4)步骤①中产生的二氧化碳气体在步骤④中得到充分的利用,从而减少了向大气中排放的量,有效保护环境.
点评 正确处理题中所提供相关信息是解答本题的关键,通过对题目所提供信息的理解与运用,才能完成本题的解答.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:初中化学 来源: 题型:选择题
| A. | 可燃物只有在空气中才能燃烧 | |
| B. | 通过降低可燃物的着火点可以灭火 | |
| C. | 空气中混有可燃性气体,遇明火可能发生爆炸 | |
| D. | 任何燃料完全燃烧时,一定会生成二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子是最小的粒子,不可以再分 | B. | 温度越高,分子运动速率越快 | ||
| C. | 分子是保持物质性质的一种粒子 | D. | 钠原子和钠离子性质相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuCl2,NaCl,K2SO4 | B. | KCl,Na2CO3,NaNO3 | ||
| C. | NaOH,Na2SO4,KCl | D. | KNO3,H2SO4,NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
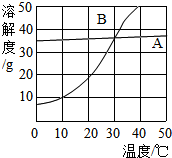 如图为A,B两种物质的溶解度曲线,下列有关说法错误的是( )
如图为A,B两种物质的溶解度曲线,下列有关说法错误的是( )| A. | 在0~30℃时,A的溶解度大于B | |
| B. | 30℃时,A、B溶液的溶质质量分数相等 | |
| C. | 使A从溶液中结晶,常用蒸发溶剂法 | |
| D. | 40℃时150g饱和B溶液降温至10℃,析出40g的B |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| B | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| C | 除去CO2中的CO | 点燃 |
| D | 区别硬水和软水 | 观察液体是否浑浊 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com