
分析 根据金属活动性顺序可知,四种金属的活动性顺序为:锌、铁、铜、银,所以向硝酸银、硝酸铜和硝酸锌的混合溶液中,加入一定量的铁粉,则铁首先与硝酸银反应生成硝酸亚铁和银,当硝酸银完全反应后再与硝酸铜反应生成硝酸亚铁和铜,不能与硝酸锌反应.向滤渣中滴加稀盐酸,无气泡产生,说明滤渣中一定不含有铁,一定含有银,可能含有铜,据此进行分析.
解答 解:由于四种金属的活动性顺序为:锌、铁、铜、银,所以向硝酸银、硝酸铜和硝酸锌的混合溶液中,加入一定量的铁粉,则铁首先与硝酸银反应生成硝酸亚铁和银,当硝酸银完全反应后再与硝酸铜反应生成硝酸亚铁和铜,不能与硝酸锌反应.向滤渣中滴加稀盐酸,无气泡产生,说明滤渣中一定不含有铁,一定含有银.溶液中一定含有的金属离子是Zn2+、Fe2+;可能发生反应的化学方程式为:Fe+2AgNO3=Fe(NO3)2+2Ag、Fe+Cu(NO3)2=Fe(NO3)2+Cu.由方程式可知,每56份质量的铁会置换出216份质量的银,每56分质量的铁能置换出64分质量的铜,所以整个反应的过程中溶液的质量减小.
故答为:Zn2+、Fe2+;减小; Fe+2AgNO3=Fe(NO3)2+2Ag(或Fe+Cu(NO3)2=Fe(NO3)2+Cu).
点评 活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属.


 阶梯计算系列答案
阶梯计算系列答案科目:初中化学 来源: 题型:选择题
 金属与盐酸的反应的示意图如图所示,下列说法正确的是( )
金属与盐酸的反应的示意图如图所示,下列说法正确的是( )| A. | 实验室可用铜和稀盐酸制氢气 | |
| B. | 四种金属中活动性最强的是镁 | |
| C. | 铁可以把锌从硫酸锌溶液中置换出来 | |
| D. | 铁与稀盐酸反应的化学方程式为:2Fe+6HCl=2FeCl3+3H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验操作 | 实验现象 |
| 向两只盛有二氧化碳气体的软塑料瓶各加入三分之一体积的水,一只静置,一只充分震荡,观察现象 | 前者无明显变化,后者瓶子变瘪 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
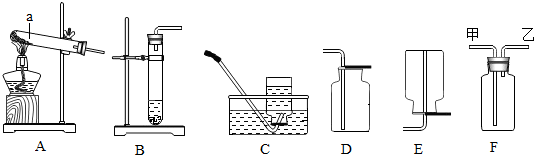
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验① | 实验② | 实验③ |
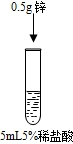 |  | 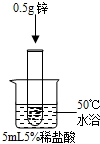 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钠不慎沾到皮肤上,立即用硫酸冲洗 | |
| B. | 一氧化碳还原氧化铁实验中,将尾气直接排放 | |
| C. | 使用酒精炉时,直接向燃着的炉内添加酒精 | |
| D. | 家中天然气泄露时.关闭阀门并打开门窗通风 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水沸腾时掀起壶盖,说明分子大小随温度升高而增大 | |
| B. | 水受热时分子间间隔变大,所占体积变大 | |
| C. | 水分解成氢气和氧气 | |
| D. | 水分子分解成氢原子和氧原子,粒子数目增多了 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com