
| 猜想 | 实验步骤 | 实验现象及结论 |
| ________ | ________ | ________ |
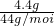 =0.1mol,故答案为:0.1mol
=0.1mol,故答案为:0.1mol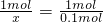 x=0.1mol
x=0.1mol 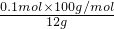 ×100%=83.3%
×100%=83.3%

科目:初中化学 来源: 题型:
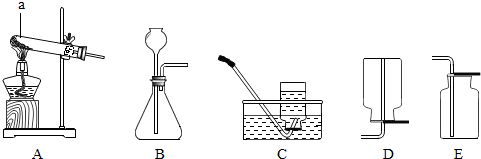
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
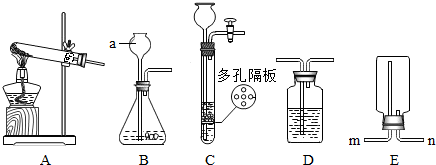
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 猜想 | 实验步骤 | 实验现象及结论 |
氯化钙和盐酸 氯化钙和盐酸 |
取少量溶液于试管中,滴加石蕊试液 取少量溶液于试管中,滴加石蕊试液 |
紫色石蕊试液变红,有盐酸和氯化钙 紫色石蕊试液变红,有盐酸和氯化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
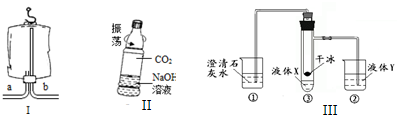
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com