
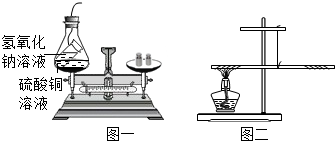
分析 【实验一】氢氧化钠溶液与锥形瓶中的硫酸铜溶液反应,有蓝色沉淀氢氧化铜产生,反应前后没有气体参加反应,也没有气体生成;【实验二】用酒精灯给左边一端铜丝加热,铜会与空气中氧气发生反应,根据反应物与生成物的比较得出实验现象,由于铜与氧气发生反应生成了氧化铜,所以左端质量大了;【结论与分析】铜丝在空气中加热,会与空气中的氧气反应生成氧化铜,所以其质量会增加.
解答 解:【实验一】氢氧化钠溶液与锥形瓶中的硫酸铜溶液反应,有蓝色沉淀氢氧化铜产生,反应前后没有气体参加反应,也没有气体生成;故填:有蓝色沉淀产生;平衡;
【实验二】(1)铜是红色固体,加热后与氧气反应生成了氧化铜,氧化铜是黑色固体,所以现象为红色固体变为黑色;铜丝原来的质量只是铜的质量,加热后变成了氧化铜,故左端的质量增加了,右端上升;
(2)反应物为铜和氧气,生成物为氧化铜,反应条件是加热,发生反应的化学方程式:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
故答案为:(1)左端铜丝表面变黑;上升;
(2)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
【结论与分析】铜丝在空气中加热,会与空气中的氧气反应生成氧化铜,所以其质量会增加,刘敏误认为反应前后反应物的总质量与生成物的总质量不一定相等.
故本题答案为:
【实验与探究】实验一:有蓝色沉淀产生;平衡;
实验二:(1)左端铜丝表面变黑;上升;
(2)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO
【结论与分析】铜丝在空气中加热,会与空气中的氧气反应生成氧化铜,所以其质量会增加.
点评 通过回答本题可知如果有质量增加的化学反应,也符合质量守恒定律,只要是质量增加了,肯定有别的物质参加了反应.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
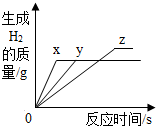 金属是重要的资源,在日常生活中已得到越来越广泛的应用.
金属是重要的资源,在日常生活中已得到越来越广泛的应用.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图所示,将小白鼠放入广口瓶中以测其呼吸作用,完成以下实验:
如图所示,将小白鼠放入广口瓶中以测其呼吸作用,完成以下实验:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 错误操作 | 不良后果 |
| ①胶头滴管取液后平放或倒持 | 液体药品流入胶帽并腐蚀胶帽 |
| ②倾倒细口瓶中的液体时,标签没向着手心 | 残液流下,腐蚀标签 |
| ③加热后的试管直接刷洗 | 试管炸裂 |
| ④实验室剩余的药品放回原瓶 | 污染试剂瓶内的试剂 |
| ⑤将一粒石灰石从竖直的试管口直接放进去 | 试管底被打破 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
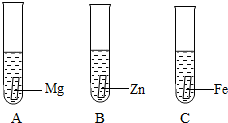 一般情况下,金属越活泼,与酸反应的速度越快.为了比较金属Mg、Zn、Fe与酸反应的快慢,某兴趣小组设计了如下的实验.
一般情况下,金属越活泼,与酸反应的速度越快.为了比较金属Mg、Zn、Fe与酸反应的快慢,某兴趣小组设计了如下的实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 工业上用赤铁矿炼铁2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ | |
| B. | 用熟石灰处理硫酸厂中的废水 Ca(OH)2+H2SO4═CaSO4+2H2O | |
| C. | 加熟石灰研磨,检验铵态氮肥Ca(OH)2+2NH4NO3═CaNO3+NH3↑+H2O | |
| D. | 用氢氧化钠制碳酸钠 Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 试管:同学们不爱惜我,我被摔碎了 | |
| B. | 铁钉:好难受啊,我在潮湿空气中生锈了 | |
| C. | 灯泡:我通电后发光了,给学生带来光明 | |
| D. | 酒精:我在空气中放置一段时间质量怎么就减轻了 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com