
| ||
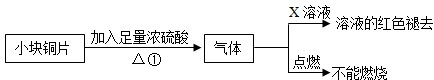
| A、需加热消耗了能源 |
| B、产生了污染空气的SO2 |
| C、降低了铜的利用率 |
| D、降低了硫酸的利用率 |
 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| ||
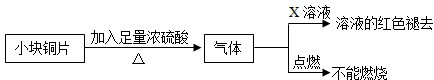
| A.需加热消耗了能源 | B.产生了污染空气的SO2 |
| C.降低了铜的利用率 | D.降低了硫酸的利用率 |
查看答案和解析>>
科目:初中化学 来源:2009年重市一中中考化学二模试卷(解析版) 题型:选择题
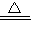 CuSO4+2H2O+SO2↑,但工业上制CuSO4并不是利用此反应,从环保角度该方法的最大缺点是( )
CuSO4+2H2O+SO2↑,但工业上制CuSO4并不是利用此反应,从环保角度该方法的最大缺点是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com