
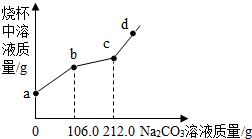
 烧杯中盛有BaCl2和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有BaCl2和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )| A. | ab段溶液变浑浊并伴有气泡 | |
| B. | bc段溶液质量增加86.3g | |
| C. | c点对应溶液的溶质质量分数为7.5% | |
| D. | d点溶液中溶质为Na2CO3 |
分析 A、根据氯化钡、盐酸中滴加碳酸钠时,碳酸钠先与盐酸反应,再与氯化钡反应考虑;
B、根据bc段是碳酸钠与氯化钡反应,根据方程式和相对分子质量计算出溶液质量的增加量;
C、c点是碳酸钠与盐酸、氯化钡恰好完全反应的点,再进行分析计算即可;
D、d点碳酸钠过量溶液显碱性考虑.
解答 解:A、氯化钡、盐酸中滴加碳酸钠时,碳酸钠先与盐酸反应,再与氯化钡反应,ab段产生气体,不能产生白色沉淀,故A错;
B、bc段是碳酸钠与氯化钡反应,与氯化钡反应的碳酸钠的质量=(212g-106g)×10%=10.6g
设碳酸钠与氯化钡反应生成沉淀质量为x则:
BaCl2+Na2CO3=BaCO3↓+2NaCl
106 197
10.6g x
$\frac{106}{10.6g}=\frac{197}{x}$
bc段溶液质量增加106g-19.7g=86.3g故B正确;
C、c点是碳酸钠与盐酸、氯化钡恰好完全反应,设碳酸钠与盐酸反应产生气体质量为y则:
2HCl+Na2CO3=H2O+CO2↑+2NaCl
106 44
10.6g y
$\frac{106}{10.6g}=\frac{44}{y}$
解得y=4.4g
c点生成氯化钠质量为z
Na2CO3-------2NaCl
106 117
21.2g z
根据$\frac{106}{21.2g}=\frac{117}{z}$
解得z=23.4g,所以c点对应溶液的溶质质量分数为:$\frac{23.4g}{100g+212g-19.7g-4.4g}$×100%=8.13%,故C错;
D、d点碳酸钠过量溶液显碱性,d点溶液中溶质为氯化钠和碳酸钠,故D错误.
故选B.
点评 解答本题关键是要知道碳酸钠先与盐酸反应,再与氯化钡反应,根据碳酸钠的质量可以计算其它物质的反应.


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:初中化学 来源: 题型:选择题
| A. | 氯化钾与氯化铵固体:加入熟石灰,研磨 | |
| B. | 硝酸铵与食盐固体:加水 | |
| C. | 氢氧化钠溶液与碳酸钠溶液:加酚酞试液 | |
| D. | 一氧化碳与氧气:通过灼热的氧化铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 结构决定性质:活性炭具有疏松多空结构,所以具有吸附性 | |
| B. | 性质决定用途:铝的化学性质比铁的稳定,所以常在铁制品表面涂铝粉防生锈 | |
| C. | 构成物质的微粒:氯化钠由钠离子和氯离子构成,所以氯化钠晶体中不存在氯化钠分子 | |
| D. | 物质的鉴别:可以用水区分硝酸铵和生石灰 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 | 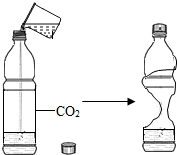 |  |  |
| A.同一物质在不同溶剂 中的溶解性不同 | B.二氧化碳与水 反应生成碳酸 | C.白磷着火点 比红磷低 | D.分子在不断运动 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com