
如图是甲、乙两固体物质的溶解度曲线,下列说法错误的是
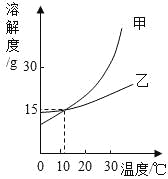
A. 10℃时,甲的溶解度小于乙的溶解度
B. t℃时,甲乙两物质的溶解度相等
C. 使甲物质从其饱和溶液中析出,可采取降温的方法
D. 甲、乙的饱和溶液从30℃降温到10℃时,析出的晶体质量甲一定大于乙
D 【解析】试题分析:由溶解度曲线可知,10℃时,甲的溶解度小于乙的溶解度,A正确;t ℃时,甲、乙两种物质的溶解度相等,B正确;甲的溶解度随温度的变化变化较大,故要提纯甲可采用降温结晶的方法,C正确;等质量的甲、乙的饱和溶液从30℃降温到10℃时,析出的晶体质量甲一定大于乙,D错误。故选D。科目:初中化学 来源:山东省临沂市2018届九年级第一次模拟考试化学试卷 题型:单选题
下列实验基本操作中,正确的是( )
A.  倾倒液体 B.
倾倒液体 B.  过滤
过滤
C.  加热液体 D.
加热液体 D.  熄灭酒精灯
熄灭酒精灯
查看答案和解析>>
科目:初中化学 来源:天津市2018届初三中考化学复习 利用化学方程式的简单计算 专题复习练习 题型:计算题
7.9g高锰酸钾完全分解,可得到氧气的质量是多少?
0.8g 【解析】设7.9g高锰酸钾完全分解,可得到氧气的质量为x 2KMnO4△ K2MnO4+MnO2+O2↑ 316 32 7.9g x =,求得x=0.8g 答:7.9g高锰酸钾完全分解,可得到氧气的质量是0.8g。查看答案和解析>>
科目:初中化学 来源:天津市2018届初三化学中考复习 氧气的实验室制取 专题训练 题型:单选题
实验室加热高锰酸钾制氧气,可直接采用的发生装置是( )

A. A B. B C. C D. D
C 【解析】试题分析:实验室中用高锰酸钾制取氧气时,反应物为固体,反应条件为加热。所以应采用固体加热制气装置,即C选项。所以应选择C项。查看答案和解析>>
科目:初中化学 来源:天津市2018届初三化学中考复习 溶液的形成及溶解度 专题训练 题型:单选题
下表是KCl和KNO3在不同温度时的溶解度。下列说法不正确的是( )
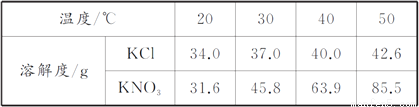
A. 20℃时,KCl的溶解度大于KNO3的溶解度
B. 两种物质溶解度相等的温度在20~30℃之间
C. 40℃时,5 gKCl中加入10 g水可得33.3%的溶液
D. 50℃时,10 gKNO3中加20 g水,充分溶解后再降温到30℃有KNO3固体析出
C 【解析】A、20℃时,KCl溶解度是34g,KNO3的溶解度是31.6g,所以20℃时,KCl溶解度大于KNO3的溶解度,正确;B、在20?30℃之间,氯化钾从34g增加到37g,硝酸钾从31.6g增加到45.8g,所以两物质溶解度相等的温度在20?30℃之间,正确;C、40℃时,氯化钾的溶解度是40g,所以10g水会溶解4g氯化钾,5gKCl加10g水可得到14g溶液,形成溶液的质量分...查看答案和解析>>
科目:初中化学 来源:天津市2018届初三化学中考复习 溶液的形成及溶解度 专题训练 题型:单选题
下列变化过程中,会吸收热量的是
A. 硝酸铵固体溶于水 B. 氢氧化钠固体溶于水
C. 木炭燃烧 D. 金属镁和稀盐酸反应
A 【解析】试题分析∶A,吸热,B,C,D,均放热。查看答案和解析>>
科目:初中化学 来源:天津市2018届九年级中考复习化学:空气 专题练习 题型:单选题
下列物质排放到空气中,不会造成大气污染的是
A. SO2 B. O2 C. CO D. NO2
B 【解析】A.SO2有毒,不能排放到空气中,否则会造成酸雨,故A错误; B.O2为空气的主要成分,排放到空气中不会造成污染,故B正确; C.CO有毒,不能排放到空气中,否则会造成环境污染,故C错误; D.NO2有毒,不能排放到空气中,否则会造成光化学污染、酸雨,故D错误; 故选:B.查看答案和解析>>
科目:初中化学 来源:天津市2018届初三化学中考复习 化学方程式 专题训练 题型:简答题
写出下列反应的化学方程式:
(1)木炭高温还原氧化铜:________________ 。
(2)铝在空气中被氧化,生成致密的氧化铝(Al2O3)薄膜:___________。
(3)铝片投入氢氧化钠溶液中,反应生成偏铝酸钠(NaAlO2)和氢气(H2):_______。
C+2CuO2Cu+CO2↑ 4Al+3O2===2Al2O3 2Al+2H2O+2NaOH===2NaAlO2+3H2↑ 【解析】本题考查了化学方程式的书写,书写时注意反应条件和配平。 (1)木炭高温还原氧化铜生成铜和二氧化碳,反应的化学方程式为:C+2CuO2Cu+CO2↑; (2)铝在空气中被氧化,生成致密的氧化铝(Al2O3)薄膜,反应的化学方程式为:4Al+3O2===...查看答案和解析>>
科目:初中化学 来源:重庆市毕业暨高中招生考试模拟(一)化学试卷 题型:计算题
在电缆产生过程中会产生一定量的含铜废料。据报道,在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜。
(1)请完成该反应的化学方程式:2Cu+2H2SO4+O2 2CuSO4+2_______
2CuSO4+2_______
(2)若选用的稀硫酸溶质的质量分数为20%,则用50g质量分数为98%的浓硫酸配制该稀硫酸,需加水_____g。
(3)某化工厂现有含铜为80%的废铜屑(假设废铜屑中杂质不参加反应),试计算制取80kg硫酸铜需要废铜屑的质量(写出计算过程及结果)____________。
H2O(1分) 196(2分) 40kg。 【解析】本题考查了质量守恒定律的应用,溶液稀释的计算和根据化学方程式的计算。理解质量守恒定律并会应用判断物质的化学式,并能依据方程式进行计算相关物质的量,明确溶液的质量=溶质的质量+溶剂的质量。 (1)根据质量守恒定律可知,在化学反应前后,原子的个数和元素的种类不变,反应前有氢元素,反应后也必须有氢元素,所以空白处为: H2O; (2)...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com