



科目:初中化学 来源: 题型:
| A、NaOH+NaHSO4═Na2SO4+H2O |
| B、CaCO3+2HCl═CaCl2+H2O+CO2↑ |
| C、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ |
| D、2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| ①用试管取少量原澄清石灰水;②取稀硫酸与碳酸钠反应来制取CO2; ③ | 步骤③中现象为 | 小明的假设不成立 |
| 实验步骤 | 实验现象 | 实验结论 |
| 将产生的气体通入硝酸银溶液 | 小亮的猜想正确 |
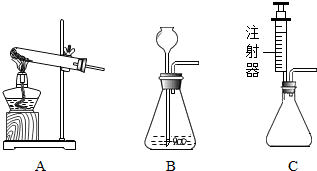
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 步骤和方法 | 现象 | 分析 | |
| 点燃前 |  | 蜡烛是白色蜡状固体,硬度小,稍有气味 |  |
| 用小刀切下一小块蜡烛投入水中 | 石蜡浮于水面 | ||
| 点燃蜡烛 |  | 蜡烛先熔化后气化,再燃烧;火焰明亮且明显分成三层 | 蜡烛熔点、沸点较低,烛焰的焰心主要是石蜡蒸气,内焰为石蜡已有部分燃烧,外焰为石蜡已完全燃烧,所以外焰温度最高. |
| 在烛焰上方罩一干燥烧杯 | 烧杯内壁出现水雾或水珠 | ||
| 在烛焰上方罩一个内壁沾有澄清石灰水的烧杯,振荡 | 烧杯内壁出现白色斑点 | ||
| 熄灭蜡烛 | 火焰熄灭,灯芯上产生一缕轻烟 | 白烟是 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
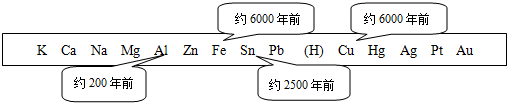
| 合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
| 焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃. |
| 硬铝 | 强度和硬度好 | 铝、铜、镁等.硬度小,质软. |
| 不锈钢 | 抗腐蚀性好 | 铁、铬、镍等.纯铁易生锈. |
查看答案和解析>>
科目:初中化学 来源: 题型:
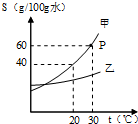 如图是甲乙两种固体物质的溶解度曲线.据图回答:
如图是甲乙两种固体物质的溶解度曲线.据图回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com