
分析 (1)根据水在通电的条件下生成氢气和氧气进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(3)根据镁和氧气在点燃的条件下生成氧化镁进行分析;
(4)根据铁和氧气在点燃的条件下生成四氧化三铁,属于化合反应进行分析.
解答 解:(1)水在通电的条件下生成氢气和氧气,化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)镁和氧气在点燃的条件下生成氧化镁,化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(4)铁和氧气在点燃的条件下生成四氧化三铁,属于化合反应,化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
故答案为:(1)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(4)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO 有可燃性和还原性 | |
| B. | CO 可用排水集气法收集 | |
| C. | CO 有毒,能跟血红蛋白结合,使人体缺氧 | |
| D. | CO 可用向上排空气法收集 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
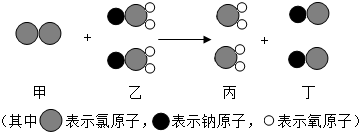 ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒.请回答下列问题:
ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 现象I | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| A取少量样品溶于水,加入过量的CaCl2溶液 | ①有白色沉淀产生 | 该反应的方程式:②Na2CO3+CaCl2═CaCO3↓+2NaCl |
| B将上述反应后的混合液过滤,取滤液③滴加稀盐酸 | ④有气泡冒出 | 证明猜想②成立 |
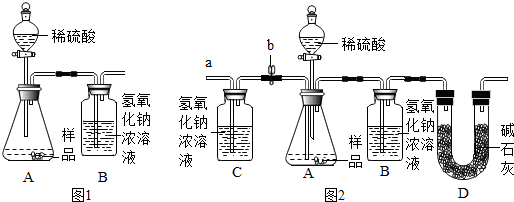
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4克 | B. | 8克 | C. | 12克 | D. | 16克 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 猜想 | 实验操作 | 现象和结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 方案一:加锌粒 | 方案二:滴加酚酞溶液 |
| 实验操作 |  | 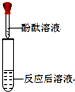 |
| 实验现象 | ⑤产生气泡 | 无明显现象 |
| 实验结论 | 溶液中有HCl | 溶液中无⑥Ca(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com