
| A、30% | B、50% | C、70% | D、90% |
| 16×3 |
| 56×2+16×3 |
| 0.3wg |
| wg |


科目:初中化学 来源: 题型:
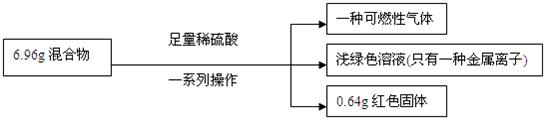
| A、生成气体质量为0.2g | B、原混合物中铁的质量分数无法计算 | C、实验中反应的H2SO4质量为10.78g | D、原混合物中铜元素的质量不一定为0.64g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案一 | 取少量滤液于试管中,滴加稀盐酸 | 没有变化 没有变化 |
猜想①成立 |
| 方案二 | 取少量滤液于试管中, 滴加稀盐酸 滴加稀盐酸 |
有白色沉淀生成 有白色沉淀生成 |
猜想②成立 |
查看答案和解析>>
科目:初中化学 来源:黄冈重点作业·初三化学(下) 题型:038
铁粉和氧化铜的混合物49.6g,放入200g盐酸中充分反应,生成H2 0.4g,然后过滤,并将滤出的固体洗涤、干燥,称得其质量为24g.再将固体用足量的盐酸处理,又生成H2 0.4g,过滤,将固体洗涤、干燥,余下固体质量为12.8g(假设第一、二次反应所生成的物质全部溶解于水).
(1)原混合物中铁粉的质量为________g.
(2)求原200g盐酸溶液中溶质的质量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com