
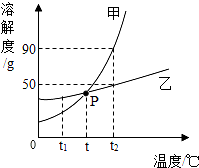
 如图为甲、乙两种物质的溶解度曲线,据图回答下列问题.
如图为甲、乙两种物质的溶解度曲线,据图回答下列问题.分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,P点表示的意义是:t1℃时,甲、乙物质的溶解度相等;
(2)t2℃时,甲物质的溶解度是90g,所以50g甲物质加入到50g水中充分溶解,形成饱和溶液,溶液质量为:95g;
(3)甲物质的溶解度受温度影响较大,所以t2℃时相同质量的甲、乙的饱和溶液降温至t1℃,析出晶体质量较多的是甲.
故答案为:(1)t1℃时,甲、乙物质的溶解度相等;
(2)饱和,95g;
(3)甲.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 20% | B. | 15% | C. | 10% | D. | 无法计算 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 鉴别氯化钠溶液和稀盐酸 | 无色酚酞 |
| B | 鉴别硫酸钠溶液和硝酸钾溶液 | 氯化钡溶液 |
| C | 除去氧化钙中少量的碳酸钙 | 加水溶解后过滤 |
| D | 除去CO2中的HCl | 碳酸氢钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
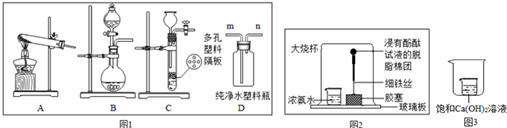
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com