
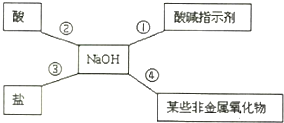
 某化学兴趣小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
某化学兴趣小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:轻巧夺冠优化训练·人教版·九年级化学下 题型:059
某化学兴趣小组以“溶液的酸碱度及其应用”为题,开展研究性学习(C),请你作为该小组成员来解决以下问题:
(1)某同学说“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性”.你认为这种推理________(填“正确”或“不正确”);
(2)从某工厂排出的废水中取出A、B两份水样,经测定,A水样的pH为4.8,B水样的pH为10.2,则A水样呈________性,B水样呈________性,A、B两份水样都对环境有污染,请设计一个实验方案帮助该工厂治理污水;
(3)氢氧化钠溶液和稀盐酸反应,无明显现象发生,请你设计一个实验,能通过清晰可见的现象,控制它们在恰好完全反应时停止实验.
查看答案和解析>>
科目:初中化学 来源:1+1轻巧夺冠·优化训练 化学 九年级下册 (人教版) 银版 人教版 银版 题型:058
某化学兴趣小组以“溶液的酸碱度及其应用”为题,开展研究性学习(C),请你作为该小组成员来解决以下问题:
(1)某同学说“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性”.你认为这种推理________(填“正确”或“不正确”);
(2)从某工厂排出的废水中取出A、B两份水样,经测定,A水样的pH为4.8,B水样的pH为10.2,则A水样呈________性,B水样呈________性,A、B两份水样都对环境有污染,请设计一个实验方案帮助该工厂治理污水;
(3)氢氧化钠溶液和稀盐酸反应,无明显现象发生,请你设计一个实验,能通过清晰可见的现象,控制它们在恰好完全反应时停止实验.
查看答案和解析>>
科目:初中化学 来源:化学教研室 题型:022
(1)为较准确地测定河水样品的酸碱度,你建议使用________(填序号)。
A.紫色石蕊试液 B.蓝色石蕊试液
C.无色酚酞试液 D.pH试纸
(2)通过网上查询,得知用于测定磷含量的试剂是钼酸铵[化学式为(NH4)2MoO4],其中钼酸铵中钼元素的化合价是________。
(3)以下几种研究方案中,你认为不恰当的是________(填序号)。
A.请教专家、老师后,进行氮、磷、钾等元素含量的测定
B.考虑到沿河建有硫酸厂,拟用氯化钡和稀硝酸检验河水中是否含有硫酸根离子
C.只到串场河上游取水样进行研究
D.调查沿河生活污水、工厂废水及化肥农药的使用情况
(4)研究报告里提出了以下设想,你认为不合理的是________(填序号)。
A.禁止沿河工厂将未处理的污水向河流中直接排放
B.城市生活污水要经处理净化达标后才能排放
C.指导农民科学合理地使用化肥、农药
D.在河流中投放化学试剂使氮、磷、钾等转化为不溶物沉降
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com