
【题目】(题文)有关物质组成及化学规律的发现对化学的发展做出了重要贡献。
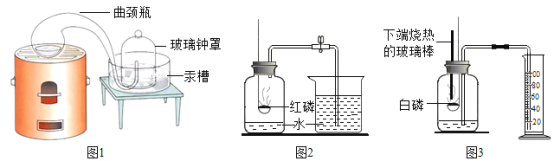
(你知道吗)二百多年前,法国化学家拉瓦锡用定量的方法研究空气成分,其中一项实验(图 1)是加热红色氧化汞粉末得到汞和氧气,该反应示意图如下:
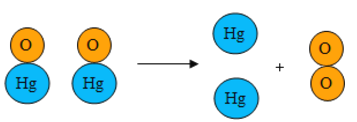
下列说法正确的是_____(填字母)
A.该反应为化合反应
B.1 个氧分子是由 2 个氧原子构成的
C.氧化汞分解过程中,原子的个数没有发生改变
D.氧化汞分解过程中,分子的种类没有发生改变
(实验回顾)实验室常用图 2 所示的方法测定空气中氧气的含量。写出红磷燃烧的符号表达式_____;实验中加入足量红磷的目的是_____.
(实验探究)同学们发现利用图 2 装置进行实验时,在集气瓶外点燃红磷,一方面会造成空气污染,另一方面伸进集气瓶速度慢了会影响测定结果。他们查阅资料发现白磷 40°即可燃烧,燃烧产物与红磷相同,于是改进装置(图 3)重新探究。先在容积为 200.0mL 的集气瓶里装进 50.0mL 的水,再在量筒内装入 100.0mL 的水, 然后按图 3 连好仪器,按下热的玻璃棒,白磷立即被点燃。
(1)集气瓶里预先装进的水,在实验过程中除了能够吸收白烟作用,还起到______、_______作用。
(2)如果白磷停止燃烧时立即记录量筒内剩余水的体积,则会导致测定的空气中氧气含量结果_____(填“偏 大”、“偏小”或“不变”)。
(拓展延伸)图 4 所示装置可用于测定空气中氧气的含量,其中与集气瓶相连的压强传感器等电子设备能将集气瓶内气体压强精确地记录并保存下来。图 5、图 6 是用该装置测得的红磷和木炭分别在集气瓶中燃烧的 压强-时间关系图(该装置气密性良好,P0 是集气瓶内初始气压,P 和 P 分别是反应结束后恢复到室温时集气瓶 内的气压。已知相同条件下集气瓶中气体的压强与气体所占的体积成正比)。
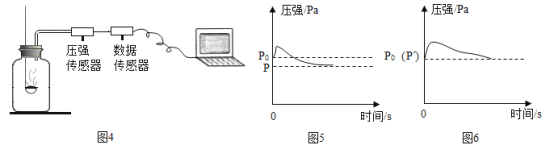
(1)根据图 5、图 6 分析,该实验中能否利用木炭燃烧测定空气中氧气含量,并说明理由_____
(2)图 5 中,根据空气中氧气的体积占总体积的 21%,可推出 P0 与 P 的关系式是______(用含 P 和 P0 的等式表示)
【答案】BCP+O2![]() P2O5;将集气瓶内的氧气充分反应加速降温、液封;偏小)不能,木炭燃烧产生二氧化碳气体,反应前后压强无变化P=79%P0
P2O5;将集气瓶内的氧气充分反应加速降温、液封;偏小)不能,木炭燃烧产生二氧化碳气体,反应前后压强无变化P=79%P0
【解析】
你知道吗:A、由图示中微粒的变化可知,是由一种物质生成两种物质,属于分解反应,故A错误;B、由图示中微粒的变化可知,1 个氧分子是由 2 个氧原子构成的,故B正确;C、由图示中微粒的变化可知,氧化汞分解过程中,原子的个数没有发生改变,故C正确;D、由图示中微粒的变化可知,氧化汞分解过程中,氧化汞分子变成了汞原子和氧分子,分子的种类发生了改变,故D错误;
实验回顾:红磷燃烧的符号表达式: P+O2![]() P2O5;测空气里氧气的含量,该实验成功的关键是红磷要过量,原因是为了耗尽集气瓶中的氧气;
P2O5;测空气里氧气的含量,该实验成功的关键是红磷要过量,原因是为了耗尽集气瓶中的氧气;
实验探究:(1)集气瓶里预先装进的水,在实验过程中除了能够加快集气瓶冷却,还起到吸收五氧化二磷的作用并形成液封;
(2) 如果白磷停止燃烧时立即记录量筒内剩余水的体积,由于温度过高而导致进入集气瓶中的水偏少,从而导致测定结果偏小;
拓展延伸:(1)该实验中不能用木炭燃烧测定空气中氧气含量,这是因为木炭燃烧生成二氧化碳气体,压强几乎不变,会导致水不能进入集气瓶;
(2) 因为氧气约占气体总体积的21%,因此P0与P的关系式是P=(1-21%)P0=79% P0。
点睛】


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:初中化学 来源: 题型:
【题目】味精是主要成分谷氨酸钠,易溶于水,其化学式是C5H8NO4Na,与硝酸银溶液不反应。味精中还含有氯化钠(味精中其他成分不考虑),氯化钠与硝酸银溶液发生复分解反应,生产氯化银白色沉淀。回答下列问题:
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是________(填字母)。
A.10mL B.50mL C.100 mL
(2)如图是配制过程,正确的操作顺序为________((填序号)。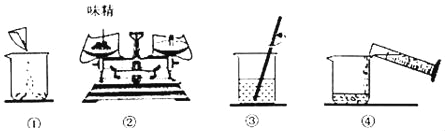
(3)为测定味精中NaCl的质量分数,进行如下实验:
在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数________((填“偏大”、“偏小”或“无影响”)
(4)为测定味精中含有氯化钠的质量分数,继续实验:
①向所配制的50g溶液中加入过量的________(溶液(填化学式)充分反应。
②然后进行________((填操作名称)、洗涤、干燥、称量白色沉淀固体。经精确测定白色沉淀的质量为2.87g,则该味精中氯化钠的质量分数为_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变?A、B、C三位同学按下面的步骤进行探究:
[提出假设]:物质发生化学变化前后总质量不变
[设计并进行实验]:A设计的实验装和选用药品如A所示,B设计的实验装置和选用药品如B所示,C设计的实验装置和药品如C所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。
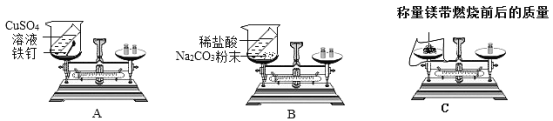
提示:A、B两个实验所发生的化学反应方程式为;
A的实验:![]()
B的实验:![]()
[实验结论]:A认为:在化学反应中,生成物的总质量等于反应物的总质量;
B认为:在化学反应中,生成物总质量小于反应物总质量;
C认为:在化学反应中,生成物总质量大于反应物总质量;
(1)你认为________的结论正确,请从原子的角度分析你认为正确的结论的原因:________.
(2)造成其它错误结论的本质原因是_______________________________;写出由此实验你得到的一点启示(或实验注意事项)在有气体参与反应时,实验装置需做哪些改进:_________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们生活在空气中,没有空气我们将无法生存,请你参与到化学兴趣小组关于气体的制取与性质的研究中,贡献你的聪明和才智。

探究一
如图1是实验室制取气体的部分装置,请回答下列问题:
氢气是最理想的燃料。通常状况下,氢气密度比空气小,难溶于水。小秦同学用锌粒与盐酸反应制取氢气,选择的装置组合是______(填字母),该发生装置的优点是____________________________,若用F装置排空气法收集氢气,气体应从___端进入(填b或c)。
探究二
(提出问题)①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
(查阅资料)无水CuSO4是白色的粉末,遇水变为蓝色;碱石灰是氢氧化钠和氧化钙的固体混合物。
(设计实验方案)小泰同学按如图2装置进行实验(假设每个装置中气体都完全反应或吸收)。
(实验现象和结论)
实验现象 | 实验结论 |
甲装置中的白色固体变成蓝色 | 气体中有H2O |
乙装置中产生______________ | 气体中有HCl |
丁装置中玻璃管内红色粉末变成黑色、戊装置中白色固体变成蓝色 | H2能与Fe2O3反应丁装置中玻璃管内反应的化学方程式为 ______ (写加热也可) |
(交流总结)
丁装置加热前通入H2的目的是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计了如下图所示的实验装置,粗略地测定空气中氧气的含量。图中烧杯内盛有80℃的热水,烧杯上方是一左端封闭、按体积均匀划分刻度的玻璃管,玻璃管内有一可左右滑动的活塞,活塞左侧玻璃管内封闭有空气,活塞右侧的玻璃管口跟空气相通,实验开始前活塞处于刻度5处。
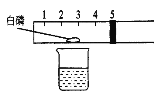
(1)实验刚开始时,玻璃管内发生的固定现象是:①____________________________;②活塞变化__________。
(2)恢复至常温后,活塞应停在刻度_____处。据此可以得出的结论是 _______________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下表:原子结构是通过科学家不断地建立与修正原子结构模型,不断地实验,不断地思考研究而得到的.下表是原子结构模型的几种学说
时间 | 模型类型 | 科学家 | 内容 |
| 道尔顿模型 | 道尔顿(英国) | 原子是一个坚硬的小球 |
| 汤姆生模型 | 汤姆生(英国) | 发现电子,即“西瓜模型”正电荷是西瓜肉,电子是西瓜籽 |
| 卢瑟福模型 | 卢瑟福(英国) | 发现原子核,原子大部分体积是空的,电子围绕带正电的原子核随意动转 |
| 分层模型 | 玻尔(丹麦) | 电子在固定轨道上分层运动(绕着原子核) |
现代 | 电子云模型 | 电子出现在原子核周围,有的区域次数多,有的区域次数少 |
![]() 上面四种原子结构模型中道尔顿的原子结构模式是________(填序号),这种原子模型是一种________结构.
上面四种原子结构模型中道尔顿的原子结构模式是________(填序号),这种原子模型是一种________结构.
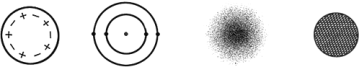
![]() 年,______通过实验发现原子结构,所做的实验名称是________,实验中大多数
年,______通过实验发现原子结构,所做的实验名称是________,实验中大多数![]() 微粒不改变原来的运动方向,顺利通过.有一小部分
微粒不改变原来的运动方向,顺利通过.有一小部分![]() 微粒发生了偏转,原因是________;极少数
微粒发生了偏转,原因是________;极少数![]() 微粒被反弹了回来,原因是________.因此,卢瑟福根据实验建立了________原子模型.
微粒被反弹了回来,原因是________.因此,卢瑟福根据实验建立了________原子模型.
![]() 请用框图的形式表示原子的结构:
请用框图的形式表示原子的结构:
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是铁丝在氧气中燃烧实验的操作图。试回答下列问题:
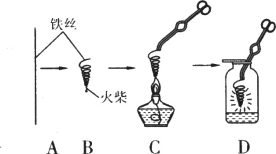
(1)B图中螺旋形铁丝的一端系一根火柴的作用是_________________。
(2)D图中集气瓶底装入少量的水,目的是_______________________。
(3)写出铁丝在氧气中燃烧的文字表达式______________________________。
(4)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录。
请你分析回答:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填写 |
你认为表中未填的实验现象是________________________________。造成铁丝在氧气中燃烧时火星四射的主要原因是________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用红磷燃烧测定空气中氧气含量的实验装置如图所示。下列有关该实验的说法正确的是
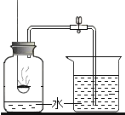
A. 红磷的量不足,导致测定结果偏大
B. 红磷燃烧时产生大量白色烟雾
C. 燃烧匙中的红磷可换成石蜡
D. 由此实验可推测氮气难溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com