
 为了测定某陨石中铁的含量,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,(杂质不与稀硫酸反应产生气体)几次试验数据如下,请回答下列问题并计算:
为了测定某陨石中铁的含量,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,(杂质不与稀硫酸反应产生气体)几次试验数据如下,请回答下列问题并计算:| 试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 所取样品的质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
| 加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
| 生成气体的质量/g | 0.2 | 0.4 | 0.5 | 0.5 |
分析 铁和稀硫酸反应生成硫酸亚铁和氢气,
由表中数据可知,在第1次实验结束后,稀硫酸完全反应;
当加入60.0g稀硫酸后,铁完全反应;
根据生成氢气的质量可以计算铁的质量,进一步可以计算陨石中铁的质量分数;
根据相关方面的数据可以画出加入稀硫酸质量与生成气体质量变化关系.
解答 解:(1)在第1次实验结束后,反应物稀硫酸完全反应完了.
故填:稀硫酸.
(2)50.0g样品与足量稀硫酸反应最多能生成气体0.5g.
故填:0.5.
(3)设铁的质量为x,
Fe+H2SO4=FeSO4+H2↑,
56 2
x 0.5g
$\frac{56}{x}$=$\frac{2}{0.5g}$,
x=14g,
陨石中铁的质量分数为:$\frac{14g}{50.0g}$×100%=28%,
答:陨石中铁的质量分数为28%.
(4)由图中数据可知,当加入50.0g稀硫酸时,铁和稀硫酸恰好完全反应,加入稀硫酸质量与生成氢气质量变化关系如下图所示: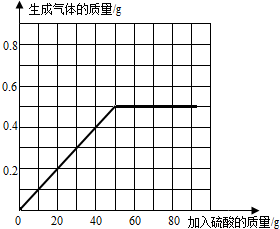
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:选择题
| A. | 异黄酮中共含有27个原子 | |
| B. | 异黄酮中含有C、H、O三种元素 | |
| C. | 异黄酮分子中含有氧分子 | |
| D. | 异黄酮中C、H、O三种元素的质量比为15:10:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实 验 步 骤 | 观察到的现象 | 实 验 结 论 |
| 取少量二氧化碳与超氧化钾反应后的固体放入试管中,然后加入盐酸 将产生的气体通入澄清的石灰水中 | 有气泡产生、 澄清的石灰水变浑浊. | 猜想③(填序号)是正确的,二氧化碳与超氧化钾反应生成的化合物是碳酸钾 (填名称). |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
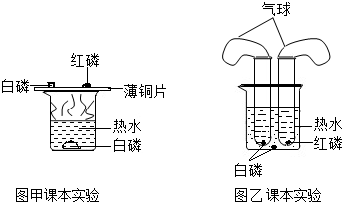 小明与同学一起对教材中“燃烧的条件”这个实验(图甲)进行了如下改进(图乙):去掉铜片,将足量的红磷和白磷分别放在两个大试管中,在试管口各自套一个气球,用线固定,然后将两支大使馆同时浸在盛有热水的烧杯中
小明与同学一起对教材中“燃烧的条件”这个实验(图甲)进行了如下改进(图乙):去掉铜片,将足量的红磷和白磷分别放在两个大试管中,在试管口各自套一个气球,用线固定,然后将两支大使馆同时浸在盛有热水的烧杯中查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
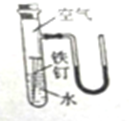 如图是某研究的实验装置,几天以后:
如图是某研究的实验装置,几天以后:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com