
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 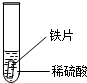 | 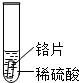 | 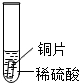 |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 铜表面无气泡 |
分析 (6)①根据题中所给化学方程式所需的条件进行分析使用酒精喷灯的原因.
②根据反应物与装置中空气的反应进行分析.
③可直接根据化学方程式进行求解.
④根据质量守恒定律可知反应后获得气体的质量为前后玻璃管内物质的质量之差.
(7)根据③问计算的二氧化碳的质量和④问计算所得的气体的质量大小进行分析解答;
(8)[作出猜想]根据三种金属的活动性顺序进行猜想;
[结论与解释]①根据实验的现象得出结论;②根据金属的表面常有一层金属氧化物会影响金属和溶液的反应分析;
[知识运用]根据在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来分析并写出反应的方程式.
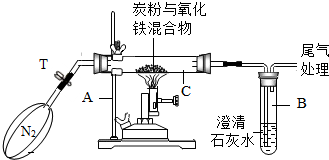
解答 解:(6)①根据反应2Fe203+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ C+C02$\frac{\underline{\;高温\;}}{\;}$2CO的反应条件为高温,可知选酒精喷灯是为了获得高温.
故答案为:获取反应所需的高温条件;
②因为反应物中碳可以在加热条件下可以和空气中的氧气发生反应生成二氧化碳,影响实验结果,所以目的就是清除试管中的空气.
故答案为:清除试管中空气(氧气),防止炭粉与空气中氧气发生反应;
③设3.20gFe2O3与炭粉发生反应生成C02的质量为x
2Fe203+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3C02↑
320 132
3.2g x
$\frac{320}{3.2g}=\frac{132}{x}$
解之得:x=1.32g
答:3.20g氧化铁完全反应时生成CO2的质量为1.32g;
④根据质量守恒定律可知:实验产物中气体质量为(48.48g+3.20g+2.00g)-52.24 g=1.44g;
答:实验中实际获得气体的质量为1.44g.
(7)因为生成的气体质量为1.44 g,大于1.32 g,故气体产物不完全为CO2,实际是C02和C0的混合物,原假设不能成立.
故答案为:不能;因为生成的气体质量为1.44 g,大于1.32 g,故气体产物不完全为CO2,实际是C02和C0的混合物,原假设不能成立(其他合理答案亦可给分).
(8)[作出猜想]三种金属的活动性顺序可能存在三种情况:猜想1为Cr>Fe>Cu;猜想2为Fe>Cu>Cr,故猜想3答案:Fe>Cr>Cu;
[结论与解释]①试管1中实验现象铁片表面产生气泡较慢,溶液变为浅绿色,可知金属铁在金属活动顺序中排在氢前,根据铬片表面产生气泡较快,溶液变为蓝色,从而得出铬也排在氢前且铬比铁活泼,因为铜不能和稀硫酸反应生成氢气,可知铜排在氢的后面,故猜想1.Cr>Fe>Cu正确;
②因为金属的表面常有一层金属氧化物会影响金属和溶液的反应,因此实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应;
[知识运用]因为金属铬比铁活泼强,故铬能和硫酸亚铁反应生成硫酸铬和铁,反应的方程式为:Cr+FeSO4=Fe+CrSO4;
故答案为:
[作出猜想]Fe>Cr>Cu;
[结论与解释]①1;②除去金属表面的氧化膜,利于反应;
[知识运用]能; Cr+FeSO4=Fe+CrSO4.
点评 本题是对金属活动性顺序的考查,运用实验探究金属的活动性顺序,考查了实验探究的过程,注重学生运用实验分析实验能力的培养.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
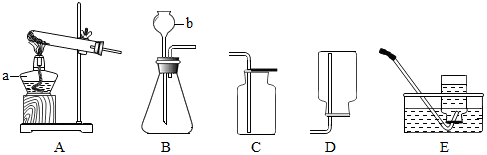
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入3~5mL5%的过氧化氢溶液,然后把试管放入盛有冷水的烧杯中 | 缓慢有少量气泡冒出 | 温度越高,过氧化氢分解的速率越大 |
| 取一支试管加入3~5mL5%的过氧化氢溶液,然后把试管放入盛有热水的烧杯中 | 迅速有大量气泡冒出 |
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 往稀酸里滴加稀氢氧化钠溶液 | B. | 向水中加入少许氢氧化钠溶液 | ||
| C. | 向稀氢氧化钠溶液中滴加稀盐酸 | D. | 往稀盐酸中滴加氯化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
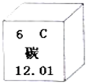 碳元素是组成许多物质的基本元素.
碳元素是组成许多物质的基本元素.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤或加热均能使硬水转化为软水 | |
| B. | 活性炭的吸附作用可使海水转化为淡水 | |
| C. | 电解水得到的H2和O2质量比为2:1 | |
| D. | 氢气在纯氧中燃烧的实验说明水由氢元素和氧元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若含碳燃料不充分燃烧火焰可能呈黄色或橙色 | |
| B. | 硫在氧气中燃烧、放热,生成了一种带有刺激性气味的气体 | |
| C. | 氧化铁与足量盐酸反应,红棕色固体减少,溶液由无色变成黄色 | |
| D. | 氢气还原氧化铜,黑色固体逐渐变成紫红色,容器内壁有水珠生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com