
分析 (1)由于不断通入足量氢气,所以氧化铜是完全转化的,进而根据氧化铜的质量求算铜的质量.
(2)由于(1)可知,应该是含有铜元素6.4g,现有质量为6.8g,则对应的是氧元素为6.8g-6.4g=0.4g.根据氧元素求对应的氧化亚铜的质量;
(3)根据氧化亚铜的质量求算生成的氯化铜的质量和铜的质量,进而求算其质量分数.
解答 解:
由于不断通入足量氢气,则氧化铜中的铜元素全部转化为单质,根据元素守恒可得,氧化铜中的铜元素的质量也就等于生成的单质铜的质量=8.0g×$\frac{64}{64+16}$×100%=6.4g
由于全部转化为红色物质,根据信息提示应该是生成了铜或者还有生成的氧化亚铜,而根据铜元素质量不变,则6.8g中铜元素的质量依旧为6.4g,所以氧元素的质量为6.8g-6.4g=0.4g
则氧化亚铜的质量为0.4g÷($\frac{16}{64×2+16}$×100%)=3.6g
设氧化亚铜完全反应生成的氯化铜的质量为x,生成的铜的质量为y.
Cu2O+2HCl═CuCl2+Cu+H2O
144 135 64
3.6g x y
$\frac{144}{3.6g}$=$\frac{135}{x}$=$\frac{64}{y}$
x=3.375g
y=1.6g
则所得蓝色溶液中氯化铜的质量分数为$\frac{3.375g}{3.6g+48.0g-1.6g}$×100%=6.75%
故答案为(1)6.4g;
(2)0.4g;3.6g
(3)6.75%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:推断题
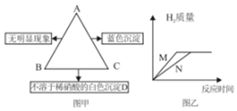 有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:
有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe→FeCl3 | B. | CaCO3→Ca(OH)2 | C. | H2O2→H2 | D. | Cu(OH)2→CuCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用淀粉溶液检验某食盐是否为加碘食盐 | |
| B. | 用湿润的蓝色石蕊试纸区别氨气和氯化氢气体 | |
| C. | 用灼烧法区别合成纤维和蚕丝 | |
| D. | 用高锰酸钾溶液区别二氧化碳和二氧化硫 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 油锅着火,立即盖上锅盖 | B. | 电器着火,立即用水扑灭 | ||
| C. | 高层住房着火,立即打开所有门窗 | D. | 沼气池清理作业前进行灯火试验 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钙的溶解度:20℃<60℃ | B. | 熔点:铜>青铜 | ||
| C. | 溶液的pH:稀氨水<稀醋酸 | D. | 热稳定性:碳酸氢铵>碳酸钙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com