
| A£® | HÖŠĒāŌŖĖŲµÄÖŹĮæĪŖ2æĖ | B£® | EĪŖŗ¬Ńõ»ÆŗĻĪļ | ||
| C£® | GŗĶHµÄ·Ö×ÓøöŹż±ČĪŖ1£ŗ2 | D£® | E·Ö×ÓÖŠŌ×ÓøöŹż±ČĪŖ1£ŗ1 |
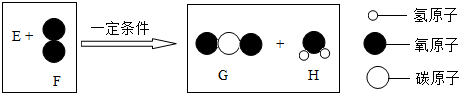
·ÖĪö A”¢øł¾Ż·Ö×Ó¹¹³ÉĶ¼Č·¶ØĪļÖŹµÄ»ÆѧŹ½£¬ĄūÓĆ»ÆѧŹ½¼ĘĖć³ö9gĪļÖŹHÖŠĖłŗ¬ĒāŌŖĖŲµÄÖŹĮ棻
B”¢ĄūÓĆĪ¢¹ŪĶ¼¼°±ä»ÆÖŠø÷ĪļÖŹµÄÖŹĮ棬ĶʶĻEĪļÖŹµÄ×é³ÉŌŖĖŲ£¬¶ŌĪļÖŹEµÄ·ÖĄą×ö³öÅŠ¶Ļ£»
C”¢ĄūÓĆ·“Ó¦ÖŠÉś³ÉĮ½ĪļÖŹµÄÖŹĮæ¼°Ī¢¹ŪĶ¼Č·¶ØĪļÖŹµÄ»ÆѧŹ½ĖłµĆµ½µÄĻą¶Ō·Ö×ÓÖŹĮ棬¼ĘĖć³öøĆ·“Ó¦ÖŠĮ½ĪļÖŹµÄ·Ö×ÓøöŹż±Č£»
D”¢øł¾ŻÉś³ÉĪļµÄ·Ö×ÓøöŹż±ČæÉĶʶĻĪļÖŹEÖŠC”¢HŌ×ÓøöŹż±Č£¬µ«ŅņŹż¾Ż²»Č«Ćę£¬ĪŽ·ØÅŠ¶Ļ·Ö×ÓÖŠŹĒ·ńŗ¬ŃõŌ×Ó£®
½ā“š ½ā£ŗÓÉÖŹĮæŹŲŗć¶ØĀÉæÉÖŖ£¬ø÷ĪļÖŹ·“Ó¦µÄĪ¢Į£øöŹż¹ŲĻµŹĒ£ŗ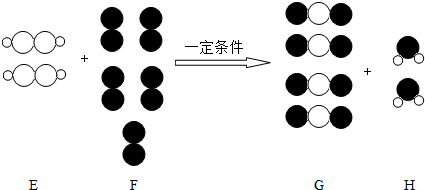
Ķعż¼ĘĖćæÉÖŖ44g¶žŃõ»ÆĢ¼ŗ¬Ńõ32g£¬9gĖ®ÖŠŗ¬Ńõ8g£¬ŗ¬Ēā1g£®ĖłŅŌæÉÖŖE²»ŗ¬ŃõŌŖĖŲ£®
A”¢H·Ö×ÓĪŖ1øöŃõŌ×ÓŗĶ2øöĒāŌ×Ó¹¹³ÉµÄĖ®·Ö×Ó£¬Ōņ9gĖ®ÖŠĒāŌŖĖŲµÄÖŹĮæ=9g”Į$\frac{1”Į2}{18}$”Į100%=1g£¬¼“9gĪļÖŹHÖŠŗ¬ĒāŌŖĖŲÖŹĮæĪŖ1g£¬¹ŹA“ķĪó£»
B”¢øł¾Ż·“Ӧɜ³ÉĪļG”¢HµÄ·Ö×Ó¹¹³ÉæÉÅŠ¶ĻĮ½ÖÖÉś³ÉĪļÖŠ¹²ŗ¬C”¢H”¢OČżÖÖŌŖĖŲ£¬¶ų·“Ó¦ĪļFÖŠÖ»ŗ¬OŌŖĖŲ£¬øł¾Ż»Æѧ±ä»ÆĒ°ŗóŌŖĖŲÖÖĄą²»±ä£¬æÉÅŠ¶Ļ·“Ó¦EÖŠŅ»¶Øŗ¬C”¢HĮ½ÖÖŌŖĖŲ£¬²»ÄÜČ·¶ØĪļÖŹEÖŠŹĒ·ńŗ¬OŌŖĖŲ£»ŌŁÓÉÉś³É44g GĪļÖŹŗĶ9g HĪļÖŹÖŠŗ¬OµÄ×ÜÖŹĮæ=44g”Į$\frac{32}{44}$+9g”Į$\frac{16}{18}$=40g£¬Čō40gŃõĘųĶźČ«·“Ó¦£¬E²»ŗ¬ŃõŌŖĖŲ£®¹ŹB²»ÕżČ·£»
C”¢ÓÉĪ¢¹ŪĶ¼£¬æÉÅŠ¶ĻGĪŖCO2”¢HĪŖH2O£¬øł¾ŻÉś³ÉGĪļÖŹ44g”¢HĪļÖŹ9g£¬½įŗĻĮ½ĪļÖŹµÄĻą¶Ō·Ö×ÓÖŹĮ棬æɼĘĖćµĆ³ö·“Ó¦ÖŠĪļÖŹGÓėHµÄ·Ö×ÓøöŹż±Č=$\frac{44g}{44}$£ŗ$\frac{9g}{18}$=2£ŗ1£»¹ŹC²»ÕżČ·£»
D”¢øł¾ŻŹ¾ŅāĶ¼æÉŅŌ擳ö£¬EÖŠŌ×ÓøöŹż±ČÓ¦øĆĪŖ1£ŗ1£®¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ “ĖĢāŅņ¶Ō·“Ó¦ĪļµÄÖŹĮæĪ“ÓŠĆ÷Č·ĖµĆ÷£¬Ņņ“ĖĪŽ·ØÅŠ¶ĻĖłŅŖĶʶĻµÄ·“Ó¦ĪļÖŠŹĒ·ńŗ¬ÓŠŃõŌŖĖŲ£¬ÓŚŹĒŹ¹ĢāÄæµÄÅŠ¶Ļ³öĻÖĮĖĘäĖüæÉÄÜŅņĖŲ£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģś øßĆĢĖį¼Ų | B£® | Ė® ¹żŃõ»ÆĒāČÜŅŗ | C£® | ĒāĘų ŅŗĢ¬æÕĘų | D£® | ŅŗŃõ ±łĖ®»ģŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | ||
| C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōµÄÄĶøÆŹ“ŠŌ | B£® | ½šŹōµÄŃÕÉ« | ||
| C£® | ½šŹōµÄÓ²¶Č | D£® | ½šŹō¼ŪøńÓėÓ²±ŅĆęÖµµÄĪĒŗĻ¶Č |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com