
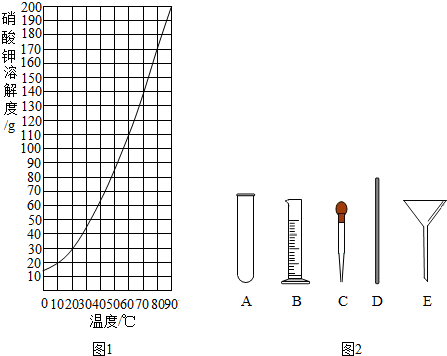
分析 (1)据溶解度曲线可知某温度下物质的溶解度,饱和溶液中溶质的质量最大,计算式$\frac{溶解度}{100g+溶解度}$×100%分析解答;
(2)溶质的质量=溶液的质量×溶质的质量分数,溶剂的质量=溶液的质量-溶质的质量,体积$\frac{质量}{密度}$;
(3)根据利用天平称量一定量物质的质量的步骤分析判断;
(4)量取液体的体积要用到量筒和胶头滴管.
解答 解:(1)由图1可知,20℃时,硝酸钾的溶解度为30g,在该温度下配制硝酸钾溶液,饱和溶液中溶质质量分数最大,$\frac{30}{130}$×100%≈23%;
(2)配制40g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为40g×10%=4g,需要水的质量40g-4g=36g,由于水的密度是1g/mL,所以需要蒸馏水的体积是36mL;
(3)要称量4g的硝酸钾,应分别在天平左右两盘放上纸片,防止药品沾在托盘上,调节平衡后,先移动游码到所需位置,再添加硝酸钾直到天平平衡;
(4)量取所需蒸馏水要用到的仪器是量筒和胶头滴管;
故答案为:(1)30; 23;
(2)4; 36;
(3)A;
(4)BC.
点评 本题考查知识比较细致、全面,因此同学们要注重平时知识的积累,才能结合选项依据所学知识正确分析和解答.


科目:初中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:3 | C. | 91:94 | D. | 1:94 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化学反应的过程是生成新物质和释放能量的过程 | |
| B. | 组成物质的元素是有限的,但有限的元素可以形成多样性的物质 | |
| C. | 控制化学反应条件就能控制化学反应,控制燃烧的条件就能控制燃烧 | |
| D. | 元素的化学性质主要取决于原子的最外层电子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ba(NO3)2、K2SO4、NaCl | B. | KCl、NaOH、CuSO4 | ||
| C. | Na2CO3、Ca(OH)2、NaNO3 | D. | NaOH、KNO3、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用浓硫酸干燥氨气 | |
| B. | 用通过灼热CuO粉末的方法除去CO2中的少量CO | |
| C. | 从MnO2与KCl的混合物中分离出KCl的方法是溶解、过滤、蒸发、结晶 | |
| D. | 只用一种试剂能鉴别出NaCl、NaOH、NH4NO3三种固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 钢筋--混合物 | B. | 生石灰--氧化物 | ||
| C. | 大理石--酸 | D. | 聚氯乙烯--有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ③②①④⑤ | B. | ③②①⑤④ | C. | ③①②⑤④ | D. | ①③②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com