
ij�����Ĺ�ҵ��ˮ�к��д�����FeSO4�Լ�һ������CuSO4��Na2SO4��Ϊ������Ⱦ�����Ϊ����ijѧϰС������������̣���Ӹ÷�ˮ�л�����������������ͭ�������ð��ԭ�����Ƽ��������ע�⣬����ҩƷ���Լ������������ֲ��P��Ӧ������ȥ��
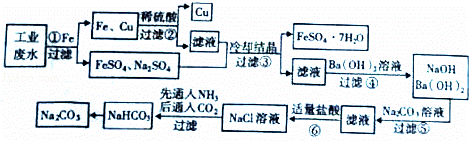
�ش��������⣺
��1���ɲ���ٿ�֪Fe��Cu�Ļ�������ǿ������˳������������������
��2������������õ���Һ�еμ�1��2����ɫʯ����Һ����Һ����������������
��3��������м�Na2CO3��Һ������������������������NaHCO3ת���ɴ���Ļ�ѧ��Ӧ����ʽΪ��������������
��4����NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl���ǰ���ƴ����е���Ҫ��Ӧ������������ȷ������������������
A�����������ʣ����Һ��ֻ��һ������
B����������NaHCO3���ܽ�ȱ�NH4Cl�Ĵ�
C��������������ҺΪNaHCO3�IJ�������Һ
D���ڼ�ѹ������������辶����ˮ��ͨ��CO2���ܼ���NaHCO3������
��5�������̢١����У������˸��ֽⷴӦ����������������������д�����ţ�
��
��1���ɲ���ٿ�֪Fe��Cu�Ļ�������ǿ������˳������Fe��Cu����
��2������������õ���Һ�еμ�1��2����ɫʯ����Һ����Һ��������������ϡ����Ļ�����Һ�Ժ�ɫ����
��3��������м�Na2CO3��Һ������������ȥ��������������NaHCO3ת���ɴ���Ļ�ѧ��Ӧ����ʽΪ��2NaHCO3 Na2CO3+H2O+CO2������
Na2CO3+H2O+CO2������
��4����NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl���ǰ���ƴ����е���Ҫ��Ӧ������������ȷ������D����
A�����������ʣ����Һ��ֻ��һ������
B����������NaHCO3���ܽ�ȱ�NH4Cl�Ĵ�
C��������������ҺΪNaHCO3�IJ�������Һ
D���ڼ�ѹ������������辶����ˮ��ͨ��CO2���ܼ���NaHCO3������
��5�������̢١����У������˸��ֽⷴӦ�������ܢݢޡ�������д�����ţ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ڿ�������������ȼ�պ��ܲ���ʹ����ʯ��ˮ����ǵ��������( )
A������ B��þ�� C����˿ D��ľ̿
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���ܱ������У�����a��CO���Ӻ�b��O2���ӣ���һ�������³�ַ�Ӧ�������ڵ�̼ԭ�Ӹ�������ԭ�Ӹ���֮����
A��a / (a+2b) B��a / 2(a+b) C��a / b D��a / 2b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ�����������ƣ�NaNO2���ж����������ʳ�μ�Ϊ���ƣ��ڸ���������ǿ���£����������ֽܷ�ų�һ�ֺ���ɫ���壬����������ǣ�������
�� A�� N2 B�� NO2 C�� O2 D�� NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Dz������ʵ��ܽ��Ա������£������ñ����ṩ����Ϣ�ش��������⣺
��1���ᡢ���֮�䷢���ĸ��ֽⷴӦ����ʵ�������ǵ���Һ������֮���������ɳ����������ˮ������Ӧ�Ͳ��ܷ�������BaCl2��Һ��NaNO3��Һ��Ϻ�����������������ܡ����ܡ����������ֽⷴӦ��
��2��д��һ����BaSO4���ɵ��кͷ�Ӧ��ѧ����ʽ��������������
OH�� NO3�� Cl�� SO42��
H+ �� �ܡ��� �ܡ��� ��
Na+ �� �� �� ��
Ca2+ �� �� ��
Ba2+ �� �� �� ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ������������( )
A��
��ȡ�Ȼ��ƹ��� B��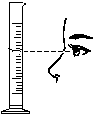
��Һ�����
C��
��ȼ�ƾ��� D��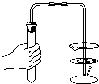
���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ǣ�C6H12O6����һ����ҪӪ�����ʣ����й��������ǵ�˵������ȷ����( )
A����������6��̼Ԫ�ء�12����Ԫ�غ�6����Ԫ�����
B����������6��̼ԭ�ӡ�12����ԭ�Ӻ�6����ԭ�ӹ���
C��ÿ�������Ƿ���������ԭ�Ӹ���Ϊ24
D��ÿ�������Ƿ�����̼���⡢��ԭ�Ӹ�����Ϊ6��1��8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����۽��Ͳ���ȷ����( )
A����ˮ�ӷ������Ӳ����˶�
B����������̼�����Ƴɸɱ��������С�����������С
C��18gˮ�д�Լ��6.02��1023��ˮ���ө����ӵ�������С
D��50mL�ƾ���50mLˮ��Ϻ������С��100mL�����Ӽ��м��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�о�С����ʵ������ȡ������̼���о��з��֣�ͨ����ѡ�ô���ʯ��ϡ���ᷴӦ��ȡ������̼����ԭ���Ƿ�Ӧ������������︲���ڹ���ı��棬�谭�˴���ʯ��ϡ����ĽӴ�����Ӧ������������ֹͣ��Ϊ�ˣ���С�������о����⣺ѡ�����Ũ�ȵ�������ʵ��ķ�Ӧ�¶���ȡ������̼��
��ʵ��һ��ѡ�����Ũ�ȵ�����
��������28��ʱ����װ��5mL������Һ��ע������ʢ��1gֱ��Ϊ2mm����ʯ�Ĵ��Թ���ע�����ᣬ��¼15�����������������������±���
�Թܱ�� 1 2 3 4 5
����Ũ�ȣ�%�� 15 20 25 30 35
���������mL�� 35 47 55 51 42
��ϡ���������ʯ��Ӧ����28��ʱ��ѡ�������Ũ�������Ϊ����%��
��ʵ�����ѡ����ʵķ�Ӧ�¶�
��������ʢ��1gֱ��Ϊ2mm����ʯ�Ĵ��Թ��зֱ����5mL��ͬ����Ũ�ȶ���ͬ�¶ȵ�������Һ���۲췴Ӧ���������¼���±���
�Թܱ�� A B C D E
�¶ȣ��棩 40 50 60 70 80
�����
�Ƚ� ���������� ���ݱ�A���Թܶ� �������Ա�B���Թܶ� �������ݲ������볣�������ᷴӦ���� ��Ӧ���ң�Ѹ�ٲ�����������
���ں��ʵ�����Ũ���£�Ӧѡ������ʵķ�Ӧ�¶�Ϊ�����棬������ʷ�Ӧ�¶�ʱ���������ʯ��Ӧ�Ļ�ѧ����ʽΪ������
�۳�ѡ���ʵ����¶Ⱥͺ���Ũ�ȵ�����֮�⣬�ڷ�Ӧ�����У�Ϊ��ֹ����Ƹ����ڴ���ʯ�ϣ�Ӧ����������������������������Ʊ���
�ܸ��о�С��Ϊ���о������Ը÷�Ӧ���ʵ�Ӱ�죬����������ʵ�飮
�Թܱ�� A B
�Թ���ҩƷ 1g��״����ʯ��5mL 25%ϡ���� 1g��ĩ״����ʯ��5mL 25%ϡ����
����ͱȽ� ���������� Ѹ�ٲ����϶�����
��������ʵ���о�������������ʹ���ʯ��Ӧ��װ���У����ѡ�����������ţ���

��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com