
科目:初中化学 来源: 题型:
| 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
| 取一定量粉末加入稀盐酸 | 没有气体产生 | 假设① |
| 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 假设② |
| 假设③ |
查看答案和解析>>
科目:初中化学 来源: 题型:
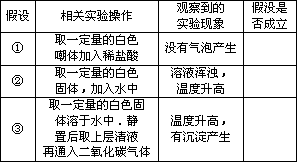
| 假设 | 相关实验操作 | 观察到的实验现象 | 假没是否成立 |
| ① | 取一定量的白色固体加入稀盐酸 | 没有气泡产生 | |
| ② | 取一定量的白色固体,加入水中 | 溶液浑浊,温度升高 | |
| ③ | 取一定量的白色固体溶于水中.静置后取上层清液再通入二氧化碳气体 | 温度升高,有沉淀产生 |
查看答案和解析>>
科目:初中化学 来源:2006年湖南省娄底市中考化学试题 题型:059
实验室有一包失去标签的白色同体物质,只知道是碳酸钠、氧化钙、氢氧化钠中的一种.为了确定其绀成,某同学大胆假设并设计实验进行探究.
[查阅资料]碳酸钠与氢氧化钙溶液反应生成氧氧化钠和碳酸钙沉淀.
[提出假设]假设①:白色固体是碳酸钠;假设②:白色固体是氧化钙;假设③:白色固体是氢氧化钠.
[实验与分析]根据假没.通过实验及分析,可作出如下判断(填表):
[拓展延伸]假定这包白色固体是混有少量氧化钙的碳酸钠,先将适量此混合物溶于足量水中,可观察到的实验现象是________,反应的化学方程式为________、________;然后将反应后的混合物进行固液分离,其分离的方法是________;再将分离后的溶液蒸干,得到的固体物质是________(填化学式).
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 假设 | 相关实验操作 | 观察到的实验现象 | 假没是否成立 |
| ① | 取一定量的白色固体加入稀盐酸 | 没有气泡产生 | ________ |
| ② | 取一定量的白色固体,加入水中 | 溶液浑浊,温度升高 | ________ |
| ③ | 取一定量的白色固体溶于水中.静置后取上层清液再通入二氧化碳气体 | 温度升高,有沉淀产生 | ________ |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省南京市玄武区九年级中考二模化学试卷(解析版) 题型:计算题
.(10分)2011年9月,某牙膏被曝含有致癌物“三氯生”而引起消费者的焦虑,于是同学们开展了对牙膏成分及作用的探究,经过查阅资料得知:
(1)很多品牌牙膏都标有“含氟”字样,其中的“氟”是指
A.氟单质 B.氟元素 C.氟原子
(2)牙膏去污主要是利用了摩擦作用。某品牌牙膏中的摩擦剂是碳酸钙,为了检验并测定牙膏中碳酸钙的质量分数,同学们取了10g牙膏,加入足量稀盐酸并搅拌。实验过程中记录并处理数据形成下图曲线:

该品牌牙膏中碳酸钙的质量分数为多少。
(3)用作牙膏摩擦剂的轻质碳酸钙可以石灰石来制备,工业上主要生产流程如下:

①“煅烧炉”中发生反应的化学方程式是: ,在“反应池”中主要发生反应的化学方程式是: 。
②“沉淀池”中生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆,熟石灰浆为
(选填“悬浊液”或“溶液”或“乳浊液”)。
③有人建议在上述流程中用CO2替代“碳酸钠溶液”。这样做的优点是 。
小王查阅资料后得知:a.二氧化碳持续通入氢氧化钙溶液发生如下反应: CO2+Ca(OH)2=CaCO3↓+H2O, CaCO3+ H2O + CO2=Ca(HCO3)2;
|
为了防止利用该法制得的轻质碳酸钙中混有Ca(HCO3)2,操作2中必需要进行的一步操作是 。
【解析】(1)运用物质是由元素组成的,“含氟”字样,其中的“氟”是指氟元素解答.
(2)由图可知碳酸钙和盐酸完全反应后生成的二氧化碳质量为1.32g,根据化学方程式列比例式求出碳酸钙的质量,进行解答
(3)煅烧炉中主要发生的是碳酸钙在高温下分解为氧化钙和二氧化碳的反应,根据化学方程式的书写规则正确书写;
沉淀池中主要发生的是氧化钙与水反应生成氢氧化钙的反应,根据化学方程式的书写规则正确书写;
根据悬浊液和乳浊液的定义进行分析回答;
用二氧化碳代替碳酸钠溶液,可达到降低生产成本和节能减排;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com