
【题目】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是元素周期表的部分内容,请认真分析并回答后面的问题:
IA | 0 | |||||||
1 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
IIA | IIIA | IVA | VA | VIA | VIIA | |||
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)很多科学家对元素周期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字:_________。
(2)请从上表中查出地壳中含量最多的金属元素的相对原子质量为__________。
(3)表中不同种元素最本质的区别是_________(填序号):
A相对原子质量不同 B质子数不同 C中子数不同
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:__________(填字母序号)、……
A从左到右,各元素原子的电子层数相同
B从左到右,各元素原子的原子序数依次增加
C从左到右,各元素原子的最外层电子数相同
(5)元素周期表中,原子序数为12的镁元素的原子结构示意图如图,该原子在化学反应中易_________(填“得到”或“失去”)电子。说明元素的化学性质与原子的_______关系密切。

【答案】门捷列夫 26.98 B AB 失去 最外层电子数
【解析】
(1)很多科学家对元素周期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字如门捷列夫。
(2)地壳中含量最多的金属元素是铝,其相对原子质量为26.98。
(3)元素是具有相同质子数的一类原子的总称,不同种元素最本质的区别是质子数不同。故选B。
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如从左到右,各元素原子的电子层数相同;从左到右,各元素原子的原子序数依次增加;从左到右,各元素原子的最外层电子数依次增加,故选AB。
(5)元素周期表中,原子序数为12的镁元素的原子结构示意图如图,该原子最外层电子数小于4,在化学反应中易失去电子。说明元素的化学性质与原子的最外层电子数关系密切。


科目:初中化学 来源: 题型:
【题目】小明同学欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸钙反应”为研究对象,设计的实验装置如图所示。
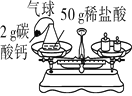
(1)根据实验目的,小明应该测量的数据是________(填“只有反应前”、“只有反应后”、“反应前、后”之一)整个反应装置(包括锥形瓶、气球和药品)的质量。
(2)实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据。
②将碳酸钙粉末全部倒入锥形瓶中,发生反应的化学方程式是___________
③当反应结束时,气球已经完全鼓起。小明发现天平的指针已经向右偏了。小明又重新称量,记录了数据。他感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符?你认为出现该实验现象的合理解释最应该是下列各项中的_____(填序号)。
A该反应前后原子的种类、数目变少
B该反应生成物的总质量小于反应物的总质量
C空气的浮力作用干扰了实验结果
D生成气体的反应不遵守质量守恒定律
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面是实验室制取气体及气体性质试验装置图.请回答下列问题:
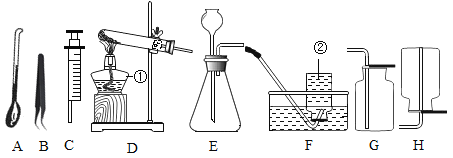
(1)写出图中仪器②的名称__________ 。
(2)实验室用高锰酸钾制取O2,应选用的发生装置为__________(填字母序号,下同), 取用高锰酸钾药品时,应选用仪器___________,写出该反应的文字表达式__________,若用F装置收集氧气,实验结束后,试管破裂,可能的原因____________。若用G装置收集,判断氧气是否收集满的方法是_______________。
(3)实验室用装置E制取氧气时,如用注射器C替换长颈漏斗,其优点是___________,发生反应的文字表达式为_______________。
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体.在通常情况下甲烷是一种无色无味的气体,难溶于水,密度比空气小.现实验室制取较纯净的甲烷应选用的发生和收集装置是 ___________________(填字母序号)。已知NO气体难溶于水,相同条件下密度略大于空气(密度与空气相近),极易与氧气反应.实验室收集NO的装置是(填字母序号)___________ 。
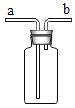
(5)实验室制取气体时,组装好仪器后进行的必要操作是:___________。若用如图装置进行排水法收集氧气,可先在装置中装满水,应从__________(填 a 或 b)端通入气体。
(6)排水法收集氧气后,测得其纯度明显偏低,原因可能是:____________(填字母,可多选)。
A高锰酸钾中混入了二氧化锰 B收集前,集气瓶中未注满水
C收集后,集气瓶中仍有少量水 D加热前就将导管伸入集气瓶
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)水是重要的自然资源。
①有关水的说法正确的是_____。
A 水是由氢元素和氧元素组成 B 水是由氢原子和氧原子构成
C 保持水化学性质的最小粒子是水分子 D 自然界的水都是纯净物
②如图为自来水厂净水过程示意图:
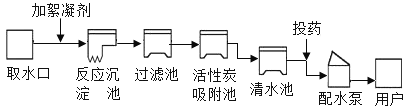
a.试剂X是_____(填名称)。
b.自来水厂的净水过程发生化学变化的一步操作是_____,经过净化操作后得到的水是硬水,鉴别硬水和软水的方法用___________,生活中将硬水转化为软水的方法是_____。
③如图是水电解实验示意图。反应的化学方程式是____________该实验中A连接电源的________极。乙管中收集的气体是______
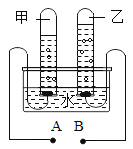
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化氢(H2O2)在二氧化锰(MnO2)作催化剂条件下,能迅速分解产生氧气,分液漏斗可以通过调节活塞控制液体的滴加速度.
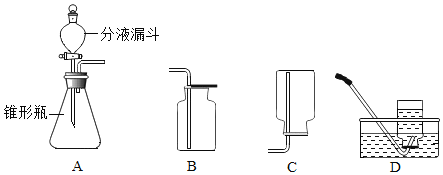
回答下列问题:
(1)分液漏斗中应放入的物质是_________,锥形瓶中应放入物质是_________;
(2)要收集一瓶纯净的氧气应选择装置_________,收集一瓶干燥的氧气应选择_________(填字母);
(3)某同学在观察到锥形瓶内有大量气泡时,开始用B装置收集氧气,过一段时间后,用带火星的木条伸入瓶口、瓶中、瓶底都未见木条复燃,其原因是_________;
(4)你认为用这个实验代替加热氯酸钾和二氧化锰混合物制取氧气,优点是_________(填编号);
a生成物只有氧气 b不需要加热 c需加热
(5)装置A中反应很剧烈,据此提出实验安全注意事项是_________(填编号)。
a控制液体滴加速度 b用体积较小的锥形瓶 c加热反应物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学用下图所示装置测定空气里氧气的含量,实验时,连接好装置并检查不漏气后再进行后续操作,下列说法正确的是( )
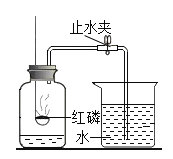
A. 所用红磷要过量,以保证集气瓶内空气里的氧气能充分反应
B. 在空气里点燃红磷后,应缓慢把燃烧匙伸入瓶内并塞紧橡皮塞
C. 红磷燃烧时,要打开止水夹,以免瓶因温度升高,气压较大,造成橡皮塞从瓶口脱落
D. 仍用本装置,只把红磷换成燃烧的本炭,能够更精确测定空气里氧气的含量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂。于是,他对影响氯酸钾分解的因素及催化剂的催化效果产生了探究兴趣。
(提出问题)氧化铜是否比二氧化锰催化效果更好?影响氯酸钾分解速率的因素有哪些呢?
(设计实验)小雨以生成等体积的氧气为标准,设计了下列几组实验。
序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
① | 10.0 g | 330 ℃ | 100 mL | t1 | |
② | 10.0 g | CuO 1.5 g | 330 ℃ | 100 mL | t2 |
③ | 10.0 g | MnO2 1.5 g | 330 ℃ | 100 mL | t3 |
④ | 10.0 g | MnO2___g | 380 ℃ | 100 mL | t4 |
(1)若t1>t2,说明氧化铜能加快氯酸钾的分解速率。若要确定氧化铜是此反应的催化剂,还需探究反应前后,氧化铜的___________和____________不变。
(2)写出实验④所涉及的化学反应的文字表达式_______。
(3)实验④中MnO2的质量为_________g,若t3>t4,则化学反应快慢与温度的关系是_____。
(4)氯酸钾的分解速率可能还与_____________因素有关。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是一种防霾新产品—鼻用空气净化器,它的填充物是硅胶,硅胶的主要成分为SiO2

(1)新鲜的空气成分中含量最高的是____
(2)SiO2读作_________
(3)下列物质中,不会造成空气污染的是____
A PM2.5 B 二氧化碳 C 二氧化硫 D 二氧化氮
(4)硅胶的结构疏松多孔,对PM2.5的吸收率达99%,说明其具有____性。有学生认为PM2.5的颗粒大小与分子大小差不多,这种说法_____(选填“正确”或“错误”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶保管不当的试剂(如下图),其残缺的标签中只剩下“Na”和“10%”的字样。已知它是无色液体,是初中化学常用的试剂。小欣和小芳同学很感兴趣,决定对其成分进行探究。

(提出猜想)
(1)这瓶试剂可能是什么溶液呢? ____
①可能是NaOH溶液; ②可能是Na2CO3溶液; ③可能是NaCl溶液。
(2)根据受损标签的情况判断,这瓶试剂不可能是____ (填字母代号)。
A酸 B碱 C盐
(收集资料)Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.测定室温(20 ℃)时,四种物质的溶解度的数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 36 | 109 | 215 | 9.6 |
(得出结论)
(3)小欣根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是_________。
(设计实验)
(4)①小芳用胶头滴管吸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是___。
②小欣为了检验该溶液是NaOH溶液还是Na2CO3溶液,她又进行了如下实验:
操作步骤 | 实验现象 | 结论及化学方程式 |
取样于试管中,滴加氢氧化钙溶液 | ___ | 猜想②正确,相关的化学方程式:_____ |
(5)请你选择与小欣不同类别的试剂,来鉴别NaOH溶液和Na2CO3溶液,你选择_______溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com