
分析 根据已有的知识进行分析,氧化铁能与硫酸反应生成硫酸铁和水;由题意Cu2O+H2SO4═Cu+CuSO4+H2O;Cu+Fe2(SO4)3═CuSO4+2FeSO4据此进行解答.
解答 解:(1)氧化铁能与稀硫酸反应生成硫酸铁和水,铜与氧气、稀硫酸反应的化学方程式2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O;故填:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O;
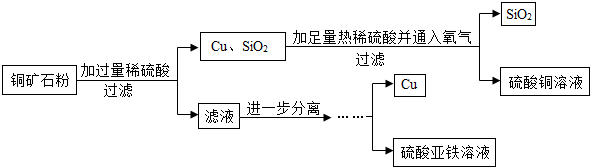
(2)铜矿石的主要成分是氧化铜,氧化亚铜,还有少量的氧化铁和二氧化硅,加过量稀硫酸充分反应后,发生以下反应①CuO+H2SO4═CuSO4+H2O;②Cu2O+H2SO4═Cu+CuSO4+H2O;③Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;所以所得滤液中的溶质有生成的CuSO4,Fe2(SO4)3,还有过量的硫酸,故填:CuSO4、FeSO4、H2SO4;
要得到铜和硫酸亚铁溶液需向滤液中加入过量铁粉,过滤,所得滤渣中加入适量稀硫酸,再过滤出铜,滤液合并为硫酸亚铁溶液.
故答案为:
(1)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O; 2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O;
(2)CuSO4、FeSO4、H2SO4;
向滤液中加入过量铁粉,过滤,所得滤渣中加入适量稀硫酸,再过滤出铜,滤液合并为硫酸亚铁溶液.
点评 本题考查了金属的性质,完成此题,可以依据已有的知识进行.注意金属的性质是中考主要考点之一.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 镁带在空气中燃烧,发出耀眼的白光,生成黑色固体 | |
| B. | 红磷在空气中燃烧,反应剧烈,产生大量白烟 | |
| C. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| D. | 硫在氧气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在氧气中燃烧发出淡蓝色火焰 | |
| B. | 硫酸铜溶液滴入氢氧化钠溶液中,产生蓝色沉淀 | |
| C. | 将生锈的铁钉放入稀盐酸中,铁锈逐渐消失,溶液颜色变为浅绿色 | |
| D. | 高温条件下木炭还原氧化铜,黑色固体逐渐变成光亮的铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
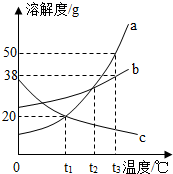 如图是a、b、c三种物质的溶解度曲线.
如图是a、b、c三种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生白色沉淀 | 反应的化学方程式为: Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想② 成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com