
 碳酸氢钠是一种重要的盐类物质,俗称小苏打,在生活中用途广泛,试举出碳酸氢钠在生活中的一种用途治疗胃酸的药物.
碳酸氢钠是一种重要的盐类物质,俗称小苏打,在生活中用途广泛,试举出碳酸氢钠在生活中的一种用途治疗胃酸的药物.分析 根据碳酸氢钠的性质推测其用途;
【实验方案1】用PH试纸检验物质的酸碱度,是较为简便的方法.只需用滴有试液的试纸与标准比色卡对比即可;碱性溶液能使紫色石蕊试液变蓝;
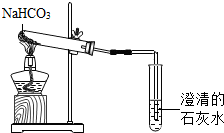
【实验方案2】根据碳酸氢钠受热分解生成了碳酸钠、水和二氧化碳解答;
【继续探究】首先假设钠离子引起溶液呈碱性,那么钠盐溶液都是呈碱性的,但根据所学知识知氯化钠溶液呈中性,说明碱性不是钠离子引起的;那么如果碳酸钠溶液呈碱性的话就一定是碳酸根离子引起的.
解答 解:碳酸氢钠是一种重要的盐类物质,俗称小苏打;碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物;受热可分解生成二氧化碳,故也可作发酵粉;
【实验方案1】根据pH试纸的使用方法进行分析.测定溶液pH的具体操作方法为:用干净的玻璃棒蘸取待测溶液并滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出相同颜色的pH值.测得溶液的pH>7,向溶液中滴加紫色石蕊试液,观察到溶液变蓝;由此得出结论是碳酸氢钠溶液呈碱性;
【实验方案2】碳酸氢钠受热分解生成了碳酸钠、水和二氧化碳,反应的化学方程式 是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
【继续探究】首先假设钠离子引起溶液呈碱性,那么钠盐溶液都是呈碱性的,但根据所学知识知氯化钠溶液呈中性,说明碱性不是钠离子引起的;那么如果碳酸钠溶液呈碱性的话就一定是碳酸根离子引起的.
所以可以设计两个实验,一是证明氯化钠溶液不显碱性,二是证明碳酸钠溶液呈碱性.可分别加入紫色石蕊试液进行鉴别,若氯化钠溶液不蓝色,碳酸钠溶液变蓝色,则证明呈碱性是碳酸根离子引起的.
取5%NaCl溶液1mL加入试管中,滴加几滴石蕊试液,石蕊试液为紫色(或不变色),Na+不会使溶液显碱性;
取5%Na2CO3溶液1mL加入试管中,滴加几滴石蕊试液,石蕊试液变蓝色,使石蕊试液变蓝色的只能是CO32-.
故答案为:
小苏打;治疗胃酸的药物;
【实验方案1】根据pH试纸的使用方法进行分析.测定溶液pH的具体操作方法为:用干净的玻璃棒蘸取待测溶液并滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出相同颜色的pH值;溶液变蓝;酸氢钠溶液呈碱性;
【实验方案2】2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
【继续探究】取5%NaCl溶液1mL加入试管中,滴加几滴石蕊试液,石蕊试液为紫色(或不变色),Na+不会使溶液显碱性;
取5%Na2CO3溶液1mL加入试管中,滴加几滴石蕊试液,石蕊试液变蓝色,使石蕊试液变蓝色的只能是CO32-.
点评 掌握碳酸盐和酸反应放出二氧化碳气体,酚酞试液的变色情况、方程式的书写,以及碳酸钠、氢氧化钠的性质,是解答的基础和关键,此外,该题还较好的考查了学生根据题意分析解决问题、应用知识解决问题的能力.


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:初中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①⑥ | C. | ①③⑥⑦ | D. | ①③⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
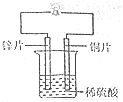 为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验.
为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验.| 锌 | 铜 | 镍 | 铜 | |
| 稀硫酸的质量分数 | 5% | 5% | 15% | 15% |
| 反应现象 | 少量气泡 | 无现象 | 许多气泡 | 无现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
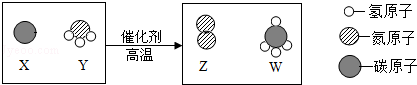
| A. | 化学反应前后元素的种类、个数、质量均保持不变 | |
| B. | W中碳元素的质量分数为75% | |
| C. | 参加反应的X、Y两物质的粒子个数比为3:4 | |
| D. | 化学反应前后元素的种类发生了变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
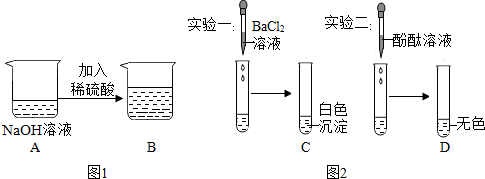
| 实验操作 | 实验现象 | 结论 |
| 取B图中的少量溶液于试管中加入紫色石蕊溶液 | 观察到紫色石蕊变红 | B图中溶液的溶质是Na2SO4和H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 甲 | 乙 | 丙 | 丁 |  |
| 分子示意图 | 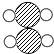 |  |  |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 白色粉末中肯定没有硫酸铜,可能有氢氧化钠和氯化钠 | |
| B. | 白色粉末中肯定有氯化钡、氢氧化钠、硫酸钠和碳酸钠 | |
| C. | 白色粉末中肯定有氯化钡、硫酸钠和碳酸钠,可能有氢氧化钠和氯化钠 | |
| D. | 若在滤液中滴加稀盐酸产生气泡,则白色粉末中肯定有碳酸钠和氯化钡,且二者的质量比可能为$\frac{{m(N{a_2}C{O_3})}}{{m(BaC{l_2})}}$>$\frac{106}{208}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com