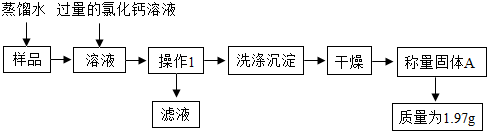
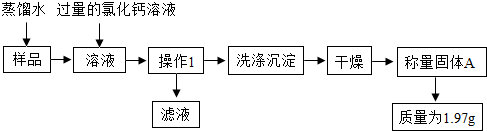
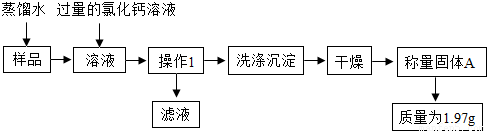
解:(1)要得到纯净干燥的一氧化碳,首先要通过烧碱除去一氧化碳中的二氧化碳,然后通过浓硫酸除去一氧化碳中的水分,因此装置连接顺序应是abcfghide或adefghibc;
(2)装置乙和丙中都盛有过量的浓烧碱,但乙和丙装置的不同点在于b和d,a导管可以连接下一个装置将气体导入,故丙装置是用来除去一氧化碳中二氧化碳的,乙装置是用来检验并吸收二氧化碳的;
(3)反应结束时还原出的铁单质高温下还可以与O
2反应,所以应使Fe在CO的还原性气氛中慢慢冷却,才能防止再被氧化.
(4)因为一氧化碳还原氧化铁实验结束时还要继续通一氧化碳直到玻璃管冷却,一氧化碳有剧毒,不能直接排放到空气中,为了保护环境,所以将排出的CO点燃;
(5)根据化学方程式中生成物CO
2的质量可求出反应物氧化铁的质量.
故答案是:(1)abcfghide或adefghibc;
(2)吸收CO
2;
(3)戊(0.5分)甲(0.5分)防止还原产生的Fe受热时被氧化;
(4)点燃 (或用气囊收集);
(5)
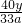
×100%或

×100%.
分析:(1)得到纯净干燥的一氧化碳应先纯净后干燥.;
(2)二氧化碳与烧碱会发生反应,从而吸收二氧化碳;
(3)Fe受热时还会被氧化;
(4)一氧化碳有剧毒,不能直接排放到空气中;
(5)乙装置增加的1.76g是生成的二氧化碳的质量,根据一氧化碳还原氧化铁的化学方程式3CO+Fe
2O
3
2Fe+3CO
2根据二氧化碳的质量可求出氧化铁的质量,进而求出铁矿石中氧化铁的质量分数.
点评:本题考查了学生对金属冶炼原理的理解程度,也考查了学生的实验能力,注重对实验现象的观察.

 CO2↑+CO↑+H2O来制取.与Fe2O3反应的CO需纯净、干燥.
CO2↑+CO↑+H2O来制取.与Fe2O3反应的CO需纯净、干燥.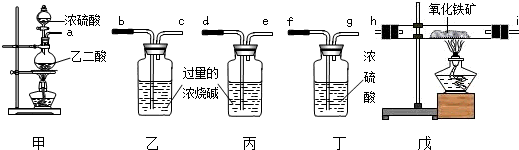
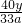 ×100%或
×100%或 ×100%.
×100%. 2Fe+3CO2根据二氧化碳的质量可求出氧化铁的质量,进而求出铁矿石中氧化铁的质量分数.
2Fe+3CO2根据二氧化碳的质量可求出氧化铁的质量,进而求出铁矿石中氧化铁的质量分数.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案