
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
分析 (1)根据溶解度的含义、饱和溶液时溶质质量分数最大、硝酸钾的溶解度随温度的升高而增大、KNO3和NaCl在20℃~30℃时具有相同的溶解度进行解答;
(2)根据饱和溶液的定义和判断方法进行分析;根据题中的数据以及题中析出晶体是通过蒸发溶剂得到的进行分析.
解答 解:(1)Ⅰ.由图表可知,20℃时,NaCl的溶解度是36g/100g水;故填:36;
Ⅱ.30℃时,饱和溶液时溶质质量分数最大,30℃时,硝酸钾的溶解度为45.8g,KNO3溶液的最大浓度(溶质质量分数)为$\frac{45.8g}{45.8g+100g}×100%$;故填:$\frac{45.8g}{45.8g+100g}×100%$;
Ⅲ.硝酸钾的溶解度随温度的升高而增大,所以从KNO3溶液中得到KNO3的一般方法是降温结晶(或冷却结晶冷却热饱和溶液);故填:降温结晶(或冷却结晶冷却热饱和溶液);
Ⅳ.根据表内数据可知,KNO3和NaCl在20℃~30℃时具有相同的溶解度,所以KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36~36.3;故填:36~36.3;
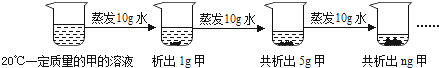
(2)Ⅰ蒸发前的烧杯底部没有固体,第一次蒸发10g水,析出1g晶体,第二次蒸发10g水共析出5g晶体,第二次蒸发10g,析出4g晶体,所以蒸发前原溶液是不饱和溶液,第三次蒸发10g水析出4g晶体,所以共析出9g;故填:不饱和;9;
Ⅱ、题中析出晶体是通过蒸发溶剂得到的,不能判断出温度对溶解度的影响,故选:C.
点评 解答本题关键是要知道溶解度的定义,溶解度曲线的意义,知道饱和溶液溶质质量分数的计算方法.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:初中化学 来源: 题型:解答题
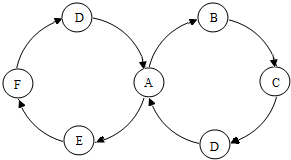 A、B、C、D、E、F是初中化学常见的六种物质,它们之间存在如下图所示的关系,箭头表示一种物质可以转化成另一种物质.已知常温下A是一种无色液体,B、C为无色无味气体;A转化成E为化合反应且放热,E、F物质类别相同,工业上用D与E反应可制取F,请回答:
A、B、C、D、E、F是初中化学常见的六种物质,它们之间存在如下图所示的关系,箭头表示一种物质可以转化成另一种物质.已知常温下A是一种无色液体,B、C为无色无味气体;A转化成E为化合反应且放热,E、F物质类别相同,工业上用D与E反应可制取F,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳分子的质量 | B. | 二氧化碳分子间间隔 | ||
| C. | 水分子间的间隔 | D. | 水分子运动速率 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酒精挥发,纸张燃烧 | B. | 用纱布滤去药渣,粮食酿酒 | ||
| C. | 镁条燃烧,铁锅生锈 | D. | 动物的呼吸作用,水分蒸发 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com