


| 实验操作 | 实验现象 | 实验结论 |
| 将燃烧后气体产物进行验证 | 甲中的白色固体变蓝 | 燃烧产物中有H2O |
| 乙装置质量增加 | 燃烧产物中有CO2,乙瓶中反应方程式2NaOH+CO2═Na2CO3+H2O | |
| 丁中玻璃管内固体红色变成黑色、戊中石灰水变浑浊 | 燃烧产物中有CO,丁中玻璃管内反应方程式 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
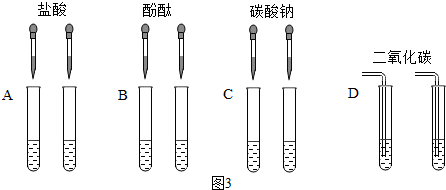
分析 (1)制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气可以用浓硫酸干燥,收集干燥的氧气必须用向上排空气法收集,不能用排水法.用无水醋酸钠(化学式为CH3COONa)和碱石灰固体混合加热制取甲烷,因此需要加热;醋酸钠与氢氧化钠反应生成甲烷和碳酸钠.由题目的信息可知:无水硫酸铜吸水后变蓝,常用于吸收水和验证水的存在,因此甲装置是检验水的,乙装置质量增加说明有二氧化碳生成,如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中有水生成,因为氢氧化钠溶液中有水;丁中玻璃管内固体颜色变化是红色变成黑色,戊中澄清石灰水变浑浊,说明生成了铁和二氧化碳,即一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;
(2)【实验方案】①根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠来分析;
②根据反应的现象进行鉴别;
③根据二氧化碳和氢氧化钙反应产生碳酸钙沉淀分析;
【猜想与假设】根据反应的程度分析溶质的成分;
【反思与拓展】根据现象得到无色澄清透明的溶液分析猜想的合理性
解答 解:(1)①用无水醋酸钠(化学式为CH3COONa)和碱石灰固体混合加热制取甲烷,因此需要加热;醋酸钠与氢氧化钠反应生成甲烷和碳酸钠;故答案为:A;
②如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气可以用浓硫酸干燥,收集干燥的氧气必须用向上排空气法收集;故答案为:CFD;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③已知“燃烧产物中有CO2”,乙瓶中为氢氧化钠溶液,故反应化学方程式为2NaOH+CO2═Na2CO3+H2O;而“丁中玻璃管内固体红色变成黑色、戊中石灰水变浑浊”,则说明气体产物中有一氧化碳,故丁中玻璃管内反应方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)【实验方案】①碳酸钠和氢氧化钙反应生成白色的碳酸钙沉淀和氢氧化钠,反应的现象为:生成白色沉淀;其化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
②A方案都反应,但都无现象,故不能鉴别;B方案都变成红色,故不能鉴别;而C和D都能出现不同的现象,因此不能达到实验目的是A、B;
③二氧化碳和氢氧化钙反应产生碳酸钙沉淀,而和氢氧化钠反应物现象,故D组实验中变浑浊的原溶液是石灰水;
【猜想与假设】若恰好完全反应,则只含有反应产生的氯化钠和氯化钙;
【反思与拓展】Ⅲ的猜想中含有氢氧化钠,能够使酚酞试液变成红色,而现象得到无色澄清透明的溶液,因此Ⅲ不合理;
故答案为:
(1)①A.
②CFD,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.③
| 实验操作 | 实验现象 | 实验结论 |
| 将燃烧后气体产物进行验证 | ||
| 2NaOH+CO2═Na2CO3+H2O | ||
| Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
点评 本考点主要考查了气体的制取装置和收集装置的选择、气体的干燥,同时也考查了化学方程式的书写等,综合性比较强;还考查了常见物质的鉴别,在做此类题时,首先弄清所要鉴别的物质的不同性质,然后选择适当的试剂进行鉴别,出现不同的现象,在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物的过量问题.


 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
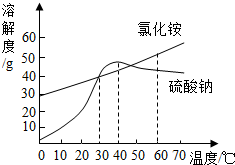 如图是氯化铵和硫酸钠的溶解度曲线示意图,由此得到的结论正确的是( )
如图是氯化铵和硫酸钠的溶解度曲线示意图,由此得到的结论正确的是( )| A. | 只有在 30℃时,两种物质的溶解度才相等 | |
| B. | 硫酸钠的溶解度随温度升高而增大 | |
| C. | 40℃时硫酸钠饱和溶液比氯化铵饱和溶液溶质质量分数大 | |
| D. | 40℃时,将硫酸钠溶液的温度升高,有晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | “低碳经济”的含义是节约能源,减少二氧化碳的排放,控制“温室效应” | |
| B. | 羊毛和棉花属于天然纤维 | |
| C. | “白色污染”可以通过一些新型的、可降解的塑料加以控制 | |
| D. | “绿色食品”是不含任何化学物质的食品 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com