
 Na2CO3+CO2↑+H2O),而碳酸钠受热不分解.现取碳酸氢钠和碳酸钠的混合物Ag,加热到质量不再改变为止,剩余的固体质量为Bg.下列说法正确的是( )
Na2CO3+CO2↑+H2O),而碳酸钠受热不分解.现取碳酸氢钠和碳酸钠的混合物Ag,加热到质量不再改变为止,剩余的固体质量为Bg.下列说法正确的是( ) g
g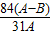 ×100%
×100% Na2CO3+H2O+CO2↑ 固体减少的质量
Na2CO3+H2O+CO2↑ 固体减少的质量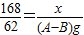
 ,
,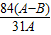 ×100%=16%,故D正确;
×100%=16%,故D正确;

科目:初中化学 来源: 题型:阅读理解
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 40.0 | 4.6 | 37.8 | 0.0 |
| 反应后质量(g) | 43.6 | 待测数据 | 4.2 | 8.8 |
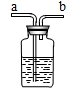
查看答案和解析>>
科目:初中化学 来源: 题型:
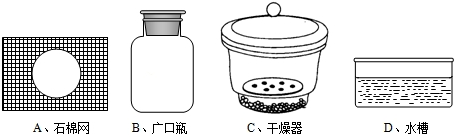
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
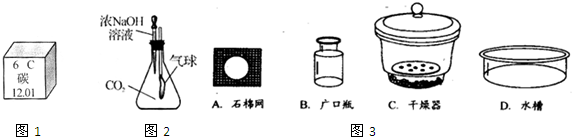
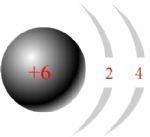
| ||
| ||
| 84(m1-m2) |
| 31(m1-a) |
| 84(m1-m2) |
| 31(m1-a) |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物或产物已略去):
A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物或产物已略去):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com