
根据国家规定,酿造食醋的总酸含量标准为
3.5 g/100 mL~5.0 g/100 mL(总酸含量即100 mL食醋中含醋酸的质量)。某兴趣小组为测定一市售食醋的总酸含量,进行了实验。实验后,得知10.0 mL该食醋样品与7.5 g溶质质量分数为4%的氢氧化钠溶液恰好完全反应。计算该市售食醋样品的总酸含量,并说明是否符合国家标准。
(醋酸和氢氧化钠反应的化学方程式:CH3COOH+NaOH=CH3COONa+H2O
假设该市售食醋样品中其他物质不与氢氧化钠发生反应)
科目:初中化学 来源: 题型:计算题
葡萄糖是生命活动中不可缺少的物质,它在人体内能直接参与新陈代谢过程。
| | 部分性质 | 生理作用 |
| 葡萄糖 化学式: C6H12O6 | 白色结晶或颗粒状粉末,味甜;易溶于水;具有还原性,葡萄糖溶液与新制氢氧化铜悬浊液反应生成砖红色沉淀 | 葡萄糖为机体所需能量的主要来源,能促进肝脏的解毒功能,对肝脏有保护作用 |

 C6H12O7+Cu2O↓+2H2O
C6H12O7+Cu2O↓+2H2O 查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6 g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5 g时,烧杯内溶液的总质量为40.3 g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算: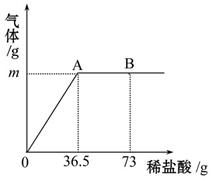
(1)A点产生气体的质量为__________;
(2)试样中碳酸钠的质量分数(结果精确到0.1%);
(3)B点时,烧杯内溶液中溶质的化学式为_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
相同质量的M、N两种活泼金属,分别与足量的稀盐酸在室温下发生反应(M、N在生成物中的化合价均为+2价),生成H2的质量m和反应时间t的关系如图所示。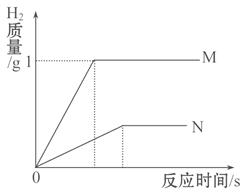
(1)金属活动性顺序是M比N________(填“强”或“弱”);相对原子质量是M比N的________(填“大”或“小”)。
(2)M与稀盐酸反应结束后,消耗稀盐酸中溶质的质量为________g。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
汽车蓄电池中稀硫酸的溶质质量分数为28%,密度为1.2克/厘米3。若要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630 克。求:
(1)630 克稀硫酸的体积是多少毫升?
(2)需要浓硫酸多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
向碳酸钠和氯化钠的混合物15.6 g中加入100 g稀盐酸,恰好完全反应后,得到111.2 g溶液。试计算:
(1)产生二氧化碳多少克?
(2)所得溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将50g木炭粉与氧化铜组成的黑色固体混合物放入试管中高温加热,待反应完成后,冷却称得剩余固体的质量为39g。试通过计算确定剩余的39g固体的组成。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室需用氯酸钾制取氧气,化学方程式: 2 KClO3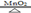 KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答:
KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答:
(1)生成氧气的质量是多少?
(2)剩余固体中氯化钾质量是多少?
(3)固体剩余物中是否还含有氯酸钾?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com