
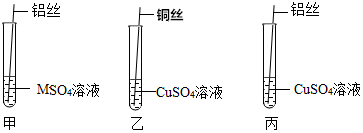
 M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.
M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu,M>Al; Al>M>Cu |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 |
分析 【提出问题】根据其余两种猜想推断第三种猜想;
【设计与实验一】根据金属与酸反应的剧烈程度进行分析;
【交流与表达】根据铝和空气中的氧气反应会生成致密的氧化铝薄膜进行分析;
【设计与实验二】(1)根据M的金属活动性大于铜的金属活动性进行分析;
(2)根据铝和硫酸铜反应生成硫酸铝和铜进行分析;
【交流与表达】根据甲、乙、丙三个实验得出的金属活动性顺序进行分析;
【评价与反思】根据金属会与酸、盐、氧气等物质反应进行分析.
解答 解:【提出问题】通过分析小敏、小强同学的猜想可知,我的猜想是M>Al>Cu;
【设计与实验一】金属越活泼,与酸反应生成氢气的反应越剧烈,所以
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu,M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| M>Al | ||||
| Al>M>Cu |
点评 验证三种金属活动性强弱关系时,通常采取“三取中”即:取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:解答题
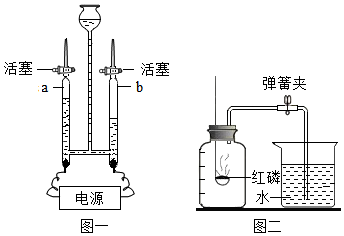 化学研究物质的组成.
化学研究物质的组成.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物 质 | 方法或试剂 |
| A | 氢气和氮气 | 点燃 |
| B | 水和过氧化氢溶液 | 二氧化锰 |
| C | 稀盐酸和稀硫酸 | 铁 |
| D | 区分黄铜(铜锌合金)和黄金 | 盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 铁丝在氧气中燃烧生成四氧化三铁 | |
| C. | 一氧化碳能够燃烧,燃烧时放出大量的热,火焰呈蓝色 | |
| D. | 将打磨过的铝丝插入硫酸铜溶液,铝丝表面有银白色物质析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
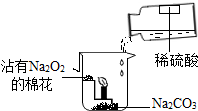 过氧化钠(Na2O2)是一种淡黄色固体,常温下与二氧化碳发生反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.现将沾有过氧化钠固体的棉花放入烧杯中,再缓慢向烧杯中倒入适量稀硫酸,使之与杯底的Na2CO3反应产生CO2气体,发现蜡烛火焰熄灭,沾有过氧化钠固体的棉花燃烧起来.从实验获得信息中,你认为不正确的是( )
过氧化钠(Na2O2)是一种淡黄色固体,常温下与二氧化碳发生反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.现将沾有过氧化钠固体的棉花放入烧杯中,再缓慢向烧杯中倒入适量稀硫酸,使之与杯底的Na2CO3反应产生CO2气体,发现蜡烛火焰熄灭,沾有过氧化钠固体的棉花燃烧起来.从实验获得信息中,你认为不正确的是( )| A. | 棉花具有可燃性 | |
| B. | Na2O2与CO2反应放热,使温度达到棉花的着火点 | |
| C. | CO2不支持蜡烛燃烧,但能支持棉花燃烧 | |
| D. | 棉花燃烧证明燃烧必须同时具备三个条件 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com