
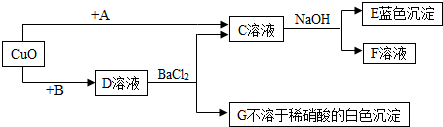
分析 (1)根据C中加入氢氧化钠蓝色沉淀判断E为氢氧化铜,C为可溶性铜盐,根据C的种类和氧化铜的性质判断A为酸,D溶液中加入氯化钡生成不溶于硝酸的白色沉淀,说明G为硫酸钡,D中含有硫酸根,则B为硫酸;结合推知C,再推导A.
(2)根据氧化铜与盐酸反应的性质以及硫酸铜溶液和氯化钡溶液反应的性质书写方程式.
解答 解:(1)D溶液中加入氯化钡生成不溶于硝酸的白色沉淀,说明G为硫酸钡或氯化银,根据D的来源,D中不可能含有银离子,故必含有硫酸根,为可溶性的硫酸盐;又因是氧化铜与B反应生成的,故D为硫酸铜,B为硫酸;硫酸铜与氯化钡反应生成硫酸钡和氯化铜,故C为氯化铜;氯化铜与氢氧化钠反应能生成蓝色的氢氧化铜沉淀和氯化钠,则E为氢氧化铜,F为氯化钠;氧化铜与A反应生成氯化铜,则A 为盐酸.
(2)C为氯化铜,E是氢氧化铜,氯化铜与氢氧化钠反应生成氢氧化铜沉淀和氯化钠,方程式为2NaOH+CuCl2═Cu(OH)2↓+2NaCl;D为硫酸铜,与氯化钡反应生成硫酸钡和氯化铜,方程式为CuSO4+BaCl2=CuCl2+BaSO4↓.
故答案为:(1)H2SO4;NaCl;BaSO4;(2)2NaOH+CuCl2═Cu(OH)2↓+2NaCl;CuSO4+BaCl2=CuCl2+BaSO4↓.
点评 物质的推断是初中化学的难重点,也是中考的热点之一,了解物质的性质是解题的前提条件,解题时还要注意前后步骤间的联系,充分利用综合归纳法得出完整合理的结论.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:初中化学 来源: 题型:选择题
| A. | CO2 | B. | SO2 | C. | ClO2 | D. | NO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
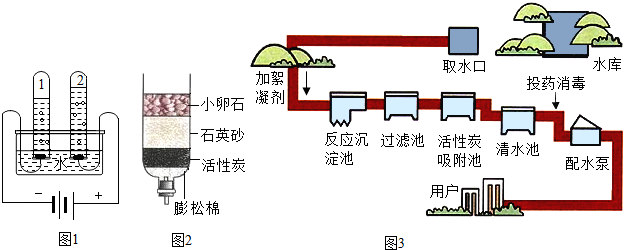
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH | B. | NaCl | C. | NH4NO3 | D. | CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
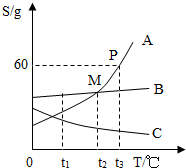 根据A、B、C三种物质的溶解度曲线,试回答下列问题:
根据A、B、C三种物质的溶解度曲线,试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组的同学想要确定A和B的成分,并测定B中氮元素的质量分数.
固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组的同学想要确定A和B的成分,并测定B中氮元素的质量分数.| 实验编号 | I | II | III | IV |
| 铵盐的质量(g) | 10.00 | 20.00 | 30.00 | 50.00 |
| 浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com