
分析 (1)根据一氧化碳和氧气的混合气点燃,可能发生爆炸进行分析;
(2)根据一氧化碳和氧化铜在加热的条件下会生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊进行分析;
(3)根据一氧化碳有毒,需要尾气处理进行分析;
(4)根据混合气体氧元素的质量分数为64%及混合物的质量为10g,求出一氧化碳的质量;
根据碳元素守恒进行计算.
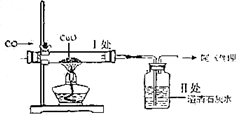
解答 解:(1)实验开始时,先通入CO一会儿,再加热,其原因是:防止一氧化碳和空气的混合气点燃,发生爆炸;
(2)一氧化碳和氧化铜在加热的条件下会生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以实验中能证明一氧化碳还原氧化铜的证据是:玻璃管中的黑色固体变成红色,澄清石灰水变浑浊;
(3)尾气处理装置通常是在导气管末端放一盏燃着的酒精灯,其作用是处理尾气,防止一氧化碳污染环境;
(4)设混合气体10g中一氧化碳的质量为x,则二氧化碳的质量为10g-x
$\frac{\frac{16}{28}×x+\frac{32}{44}×(10g-x)}{10g}$×100%=64%
x=5.6g
CO和CO2的混合气体10g,且知该混合气体中含氧64%,所以碳元素的质量为:10g×(1-64%)=3.6g
生成碳酸钙质量为:$\frac{3.6g}{12%}$=30g,故选:C.
故答案为:(1)防止一氧化碳和空气的混合气点燃,发生爆炸;
(2)玻璃管中的黑色固体变成红色,澄清石灰水变浑浊;
(3)处理尾气,防止一氧化碳污染环境;
(4)5.6g,C.
点评 本题主要考查了一氧化碳还原氧化铁的操作和注意事项,难度不大,需要在平时加强记忆.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
 某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.生成的是什么气体呢?同学们决定进行探究.探究前老师提示,该反应生成的气体只有一种.
某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.生成的是什么气体呢?同学们决定进行探究.探究前老师提示,该反应生成的气体只有一种.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次 数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 固体减少质量/g | 1.8 | 1.8 | m | 0.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X、Y、Cu | B. | Y、Cu、X | C. | Y、X、Cu | D. | X、Cu、Y |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 木炭在氧气中燃烧发出白光 | |
| B. | 细铁丝在氧气中剧烈燃烧,火星四射,生成一种白色物质 | |
| C. | 镁条在空气中燃烧发出耀眼的白光并放出大量的热 | |
| D. | 硫在空气中燃烧发出淡蓝色火焰,生成有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com