
| 实验操作 | 现象 | 结论 | |
| 方案一 | 取少量待测溶液于试管中,通入CO2 | 出现白色沉淀 | 氢氧化钠溶液中含有氢氧化钙 |
| 方案二 | 取少量待测溶液于试管中,请加 Na2CO3溶液 | 出现白色沉淀 |

| 实验操作 | 现象 | 结论 |
| 取少量沉淀C于试管中,加入过量 稀盐酸. | 有气泡产生,沉淀全部消失. | 白色固体样品中一定含有 碳酸钠. |
分析 实验一:【分析】根据碱具有相似化学性质的原因,进行分析解答.
【设计方案并实验】根据氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,氢氧化钙能与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,进行分析解答.
【方法感悟】根据物质的性质决定物质的检验方法,进行分析解答.
实验二:(1)根据过滤操作所需的仪器,进行分析解答.
(2)根据溶于水形成无色溶液,滴加酚酞溶液变红色,加入过量氯化钡溶液生成沉淀,向红色溶液中滴加过量的稀硝酸和硝酸银溶液,得到无色溶液和沉淀,说明沉淀不溶于稀硝酸,应为硫酸钡或氯化银沉淀,进行分析解答.
(3)根据沉淀C可能是碳酸钡或硫酸钡,碳酸钡能与稀盐酸反应生成二氧化碳气体,硫酸钡不与酸反应,进行分析解答.
(4)根据碳酸钠与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,进行分析解答.
解答 解:实验一:【分析】氢氧化钙和氢氧化钠都属于碱,它们在水溶液中都能解离出相同的氢氧根离子,其离子符号为:OH-.
【设计方案并实验】氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,氢氧化钙能与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式分别是CO2+Ca(OH)2═CaCO3↓+H2O、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【方法感悟】在检验物质时,要分析物质的组成和性质,据此选择加入恰当的试剂,最后根据不同现象得出结论.
实验二:(1)过滤操作用到的玻璃仪器有:烧杯、玻璃棒和漏斗.
(2)白色固体溶于水形成无色溶液,说明不能同时含有硝酸钡和碳酸钠、硫酸钠,因为硝酸钡和碳酸钠、硫酸钠反应能生成碳酸钡、硫酸钡白色沉淀.
滴加酚酞溶液变红色,说明溶液显碱性,含有碳酸钠或氢氧化钠中的一种;加入过量氯化钡溶液生成沉淀,说明含有碳酸钠、硫酸钠中的一种,则白色固体中一定不含硝酸钡.
向红色溶液中滴加过量的稀硝酸和硝酸银溶液,得到无色溶液和沉淀,说明沉淀不溶于稀硝酸,应为硫酸钡或氯化银沉淀.
(3)沉淀C可能是碳酸钡或硫酸钡,碳酸钡能与稀盐酸反应生成二氧化碳气体,硫酸钡不与酸反应,取少量沉淀C于试管中,加入过量稀盐酸,有气泡产生,沉淀全部消失,说明沉淀全部是碳酸钡,一定不是硫酸钡,即说明原混合物中一定含有碳酸钠,一定不含硫酸钠.
(4)小虎同学认为白色固体中还有物质不能确认其是否存在,是因为碳酸钠与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,反应的化学方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl.
如要确认,只需将上述实验方案中所加的一种试剂改为硝酸钡溶液即可,碳酸钠与硝酸钡溶液反应生成碳酸钡沉淀和硝酸钠,不影响氯化钠的测定.
故答案为:实验一:【分析】OH-;
【设计方案并实验】CO2+Ca(OH)2═CaCO3↓+H2O(或Ca(OH)2+Na2CO3═CaCO3↓+2NaOH).
【方法感悟】性质.
实验二:(1)漏斗;(2)硝酸钡;(3)稀盐酸;(4)BaCl2+Na2CO3═BaCO3↓+2NaCl;硝酸钡溶液.
点评 本题难度较大,熟练掌握盐的化学性质、碱的化学性质、化学方程式的书写方法、常见物质的检验方法等是正确解答本题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应时间/s | 0 | 10 | 20 | 30 | 40 |
| 烧杯及其溶液的质量/g | 90.2 | 88.1 | 85.2 | 83.8 | 83.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
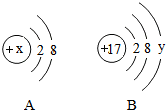 (1)化学用语是学习化学的基本工具,请用化学符号填空:
(1)化学用语是学习化学的基本工具,请用化学符号填空:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com