
【题目】如图所示,在电解水的实验中,通电一段时间后,若A试管中收集到了10mL的气体,则B试管中应同时收集到mL的气体. 
①A试管中产生的气体是 , B试管中产生的气体是 , 由此证明电解水时发生了变化,该变化的文字表达式为 , 基本反应类型是 .
②已知化学变化前后元素种类不变,那么由此实验可得出水是由组成的.
【答案】5;氢气(H2);氧气(O2);化学;水 ![]() 氢气+氧气;分解反应;氢元素和氧元素
氢气+氧气;分解反应;氢元素和氧元素
【解析】解:试管收集的气体较多接负极是氢气,A试管和B试管中收集到的气体的体积比约等于2:1.所以若A试管收集到10ml的气体,则B试管收集到气体的体积是5ml;故填:5;
通电一段时间后,A试管中收集到的气体是氢气,B试管中收集到的气体是氧气,A试管和B试管中收集到的气体的体积比约等于2:1.由此证明电解水时发生了化学变化,此实验说明水是由氢元素和氧元素组成.水在通电的条件下生成氢气和氧气,该变化的文字表达式为:水 ![]() 氢气+氧气;属于由一种物质生成两种物质的分解反应;(2)水在通电的条件下生成氢气和氧气,此实验说明水是由氢元素和氧元素组成.
氢气+氧气;属于由一种物质生成两种物质的分解反应;(2)水在通电的条件下生成氢气和氧气,此实验说明水是由氢元素和氧元素组成.
答案:5; ①氢气(H2); 氧气(O2); 化学;水 ![]() 氢气+氧气; 分解反应; ②氢元素和氧元素;
氢气+氧气; 分解反应; ②氢元素和氧元素;
【考点精析】解答此题的关键在于理解电解水实验的相关知识,掌握电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:初中化学 来源: 题型:
【题目】某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究: 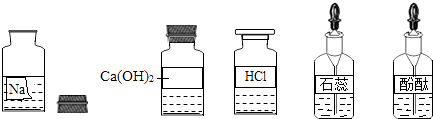
【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;
猜想三:碳酸钠溶液.
【实验推断】
(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是溶液,理由是;
(2)小刚另取样滴加稀盐酸有产生,反应的化学方程式为 , 小刚得出结论:该溶液是碳酸钠溶液.
(3)小青认为小刚的结论不完全正确,理由是 . 小组同学讨论后一致认为还需要进行如下实验: 【继续探究】另取样加入过量的CaCl2溶液,观察到有产生,设计这一步骤的目的是;静置后,取上层清液,滴入酚酞试液,溶液呈红色.
【实验结论】这瓶溶液是 .
(4)【探究启示】实验取完药品后应 . 【拓展迁移】若该溶液与盐酸发生中和反应,恰好完全反应的微观过程如图所示,反应的实质表达式为:H++OH﹣=H2O,则反应后溶液中存在的阴、阳离子是
(填符号);
【继续探究】实验中加CaCl2溶液反应的实质表达式:(用化学符号表示)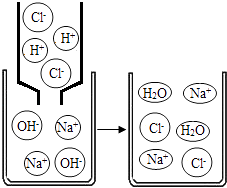
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】柠檬酸(C6H8O7)在水溶液中可以解离出H+,从而呈现酸性,主要用于香料或作为饮料的酸化剂,下列物质不能与柠檬酸反应的是
A. CO2 B. Fe2O3 C. Mg D. NaOH
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语(化学符号)表示:
(1)空气中体积分数最大的气体
(2)2个氖原子
(3)5个二氧化碳分子
(4)3个镁离子
(5)氧化铁中铁元素的化合价
(6)2个硝酸根离子 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿矾(FeSO47H2O)是硫酸法生产太白粉的主要副产物,可用于制备Fe2O3 , 复印用Fe3O4粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作.某研究性小组展开了系列研究. Ⅰ制备Fe2O3
【资料一】
①无水硫酸铜遇水变成蓝色的硫酸铜晶体.
②绿矾(FeSO47H2O)高温分解产生一种金属氧化物和几种气态非金属氧化物.
③SO2是无色有窒息性臭味的有毒气体,能使品红溶液褪色.
甲同学用如下装置制备Fe2O3并验证绿矾受热分解的其他产物;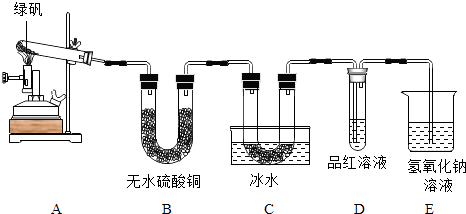
(1)实验过程中发现:A中有色固体生成,B中无水硫酸铜变蓝,C中U形管内有无色晶体(SO3)析出,D中品红溶液褪色,装置E的作用是 , 绿矾高温分解的化学方程式为 .
(2)Ⅱ制备Fe3O4 乙同学模拟生产复印用Fe3O4粉的实验流程如下: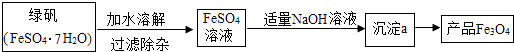
【资料二】Fe(OH)2是一种白色难溶于水的固体,在空气中易被氧化.
FeSO4溶液中加入NaOH溶液,反应的化学方程式依次为① , ②4Fe(OH)2+O2+2H2O═4Fe(OH)3 . 由沉淀a获得Fe3O4的化学方程式为:Fe(OH)2+2Fe(OH)3═Fe3O4+4H2O
若制取Fe(OH)2 , 采取的实验操作是:向盛有5mL新制FeSO4溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶O2),胶头滴管的争取使用方法是(填字母).
(3)Ⅲ制备还原铁粉 制备还原铁粉的工业流程如下: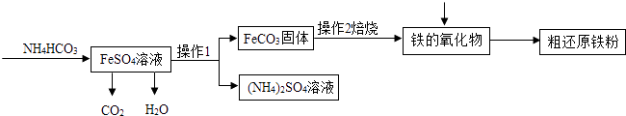
①操作1的名称是 , NH4HCO3和FeSO4溶液反应的化学方程式为 .
②若将14.06g粗还原铁粉(假设粗还原铁粉中杂质仅含少量FexC)在氧气流中完全反应,得到0.22g
CO2 , 将相同质量的粗还原铁粉与足量稀硫酸反应,得到0.48gH2(FexC与稀硫酸反应不产生H2).试通过计算确定FexC的化学式(请写出计算过程) .
③粗还原铁粉经加工处理后变成纯还原铁粉,纯还原铁粉和水蒸气在高温条件下也可制得四氧化三铁,同时生成一种气体.其装置如图所示: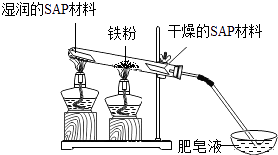
SAP材料吸水性强,湿润的SAP材料能为该反应持续提供水蒸气.实验开始一段时间后,观察到在肥皂液中有大量的气泡产生,此气泡用火柴即能点燃,同时有肥皂泡飘到空中.生成的气体是 , 干燥的SAP材料作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com