
分析 根据已有的氢氧化钠的性质、二氧化碳能与氢氧化钠反应生成碳酸钠和水、化学反应前后原子的种类和个数不变解答即可.
解答 解:(1)氢氧化钠能与空气中的二氧化碳反应生成碳酸钠和水,故填:与空气中的二氧化碳反应;2NaOH+CO2═Na2CO3+H2O;
(2)SiO2+2NaOH═X+H2O,反应前含有1个Si原子,4个O原子,2个Na原子和2个H原子,反应后含有2个H原子和1个O原子,故X中含有2个Na原子,1个Si原子,3个O原子,故其化学式为Na2SiO3,故填:Na2SiO3.
点评 本题考查的是常见的碱的性质、化学方程式的书写以及质量守恒定律的应用,完成此题,可以依据已有的知识进行.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
| 实验数据 | 反应前 | 反应后 | |
| 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和反应后混合物的质量 | |
| 300g | 24g | 315.2g | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
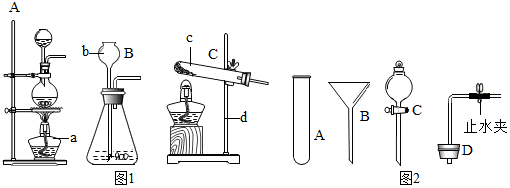
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量的该漂白液加入到烧杯中,再放入有色布条 | 一段时间后,有色布条没有变化 | 该漂白液已完全失效 |
| 实验操作及实验现象 | 实验结论 |
| 取少量该漂白液于试管中,加入过量的稀盐酸.观察到有气泡产生 | 猜想①不合理 |
| 取一定量的漂白液于试管中,加入过量的CaCl2溶液使Na2CO3完全反应,静置后向上层清液中滴加酚酞溶液,无明显变化 | 猜想③不合理,②合理 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
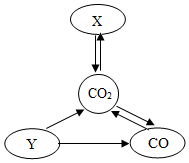 如图可用来表示C、CO、CO2、CaCO3四种物质间的相互转化关系,分析回答问题
如图可用来表示C、CO、CO2、CaCO3四种物质间的相互转化关系,分析回答问题查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状提出问题,并在实验室进行了以下探究.
淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状提出问题,并在实验室进行了以下探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 冰雪融化 食物腐烂 | B. | 牛奶变酸 铁生锈 | ||
| C. | 水的电解 纸张燃烧 | D. | 酒精挥发 工业上制氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com