
| 温度(℃) | 10 | 40 | 65 | 75 |
| 剩余固体(g) | 261 | 175 | 82 | 82 |
| 温度(℃) | 10 | 40 | 50 | 55 | 60 | 65 | 75 | 80 |
| 溶解度(g) | 20.9 | 63.9 | 85.5 | 95 | 110 | 126 | 150 | 169 |
分析 (1)根据升温后又溶解的硝酸钾的质量和升温后溶解度增加的质量进行分析即可;(2)根据升温到75℃时的溶解度变化可知,现在硝酸钾已经全部溶解完,72g全部是杂质,再根据10℃溶解的硝酸钾质量加上升温后溶解的硝酸钾的质量即可
解答 解:(1)根据40℃剩余物质175g,再升温到65℃,剩余物质又少了,说明升温到40℃时,固体中还含有硝酸钾;该物质由10℃升温到40℃,又溶解了261g-175g=86g,由10℃升温到40℃硝酸钾的溶解度增加了63.9g-20.9g=43g,即100g水中能多溶解43g,又因为升温后溶解了86g,所以加入水的质量200g;
(2)40℃升温到75℃时的溶解度增加了150g-63.9g=86.1g,所以200g水中还能溶解2×86.1g=172.2g,但实际溶解了175g-82g=93g,说明硝酸钾已经全部溶解完,所以82g全部是杂质,由10℃升温到75℃,共溶解硝酸钾质量为261g-82g=179g,10℃溶解硝酸钾质量为2×20.9g=41.8g;所以原固体混合物中含有硝酸钾的总质量为:179g+41.8g=220.8g.
故答案为:(1)200g;(2)220.8g.
点评 解答本题关键是要知道升温后又溶解了多少溶质,升温后溶解度的变化情况分析出原来溶液中溶剂的质量,再进一步进行分析即可.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
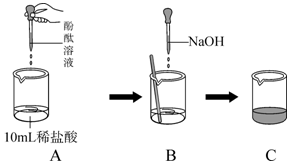
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
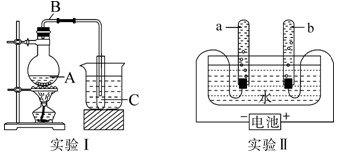
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①②③ | C. | ①②③⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 内容 装置 | 【实验1】制备气体 | 【实验2】测定气体含量 |
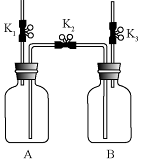 | Ⅰ.打开K1,用注射器向盛有锌粒的A中注入稀硫酸,直至液面浸没下端导管口 Ⅱ.在K1上方导管口收集气体 | Ⅰ.A(容积350ml)中为用排空气法收集的CO2,B中装满水.用注射器向A中注入15mL NaOH溶液(足量),充分反应 Ⅱ.打开K2和K3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
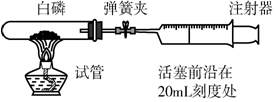 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com