
 已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热能分解生成碳酸钙和一种有毒气体,碳酸钙高温分解生成氧化钙和二氧化碳.草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4),相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4
已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热能分解生成碳酸钙和一种有毒气体,碳酸钙高温分解生成氧化钙和二氧化碳.草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4),相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4| 步骤 | 实验操作 | 实验现象 | 结论 |
| I | 取少量固体放入烧杯中,加适量水并搅拌,静置后,取上层清液于试管中,滴加无色酚酞溶液. | 溶液不变红. | 剩余固体中一定不含有氧化钙 |
| II | 另取少量固体放入试管中,加足量稀盐酸 | 有气体产生,固体全部溶解 | 剩余固体中一定含有CaCO3;可能含有CaC2O4. |
分析 (1)图中t1~t2段发生的反应是草酸钙受热分解生成碳酸钙和一氧化碳;t4~t5段是碳酸钙完全反应后的固体,即固体是氧化钙;
(2)氧化钙和水反应生成氢氧化钙,氢氧化钙溶液能使无色酚酞溶液变红解答;碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)图中t1~t2段发生的反应是草酸钙受热分解生成碳酸钙和一氧化碳,反应的化学方程式为:CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑;
t4~t5段是碳酸钙完全反应后的固体,即固体是氧化钙.
(2)探究草酸钙加热一段时间后剩余固体M的成分如下表所示:
| 步骤 | 实验操作 | 实验现象 | 结论 |
| I | 取少量固体放入烧杯中,加适量水并搅拌,静置后,取上层清液于试管中,滴加无色酚酞溶液. | 溶液不变红. | 剩余固体中一定不含有氧化钙 |
| II | 另取少量固体放入试管中,加足量稀盐酸 | 有气体产生,固体全部溶解 | 剩余固体中一定含有 CaCO3;可能含有 CaC2O4 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:实验探究题
| 实验编号 | 实验操作 | 实验现象 |
实验① | 取10mL5%的过氧化氢溶液于试管中,过一会儿把带火星的木条伸入试管中 | 有少量气泡产生,木条不复燃 |
实验② | 取10mL5%的过氧化氢溶液于试管中,加入少量二氧化锰,把带火星的木条伸入试管中 | 有大量气泡产生,木条复燃 |
| 实验编号 | 实验操作 | 实验现象 |
实验③ | 取10mL蒸馏水于试管中,加入少量二氧化锰,把带火星的木条伸入试管中 | 无气泡产生,木条不复燃 |
| 实验编号 | 实验药品 | 分解温度(℃) |
| 实验④ | 1.2gKClO3 | T1 |
| 实验⑤ | 1.2gKClO3、0.5gMnO2 | T2 |
| 实验⑥ | 1.2gKClO3、0.5gFe2O3 | T3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 化学方程式 | 反应类型 | |
| A | H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+O2↑ | 分解反应 |
| B | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 置换反应 |
| C | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | 化合反应 |
| D | H2SO4+2NaOH═Na2SO4+2H2O | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 能表示一个分子的是①④⑥ | |
| B. | ④中的数字“5”表示五氧化二磷中有5个氧原子 | |
| C. | 表示物质组成的化学式是③④⑥ | |
| D. | ②⑤的质子数相同,化学性质也相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质的组成与性能 | 用于食品添加剂 | |||
| 物质名称 | 物质组成 | 主要化学性质 | 作用 | 法律规定 |
| 碳酸氢钠 | NaHCO3 | 无毒、弱碱性,易与酸反应,受热分解成碳酸钠、水和二氧化碳 | 膨松剂 | 可用 |
| 食盐 | NaCl | 易溶、中性,与硝酸银溶液反应生成白色沉淀 | 调味剂 | 可用 |
| 甲醛 | CH2O | 有毒,能使人体中蛋白质失去生理活性 | 防腐 | 国家严禁使用 |
| 亚硝酸钠 | NaNO2 | 易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 | 发色剂、防腐剂 | 严格依据国家标准 |
| 铁 (还原性铁粉) | Fe | 比较活泼的金属,能与胃液反应 | 抗氧化剂 | 依据国家标准可用 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 “淮南牛肉汤”是淮南小吃,选用沿淮黄牛肉、千张、豆饼、红薯粉丝、辣椒油等为主原料,配上香料、高汤等辅料制作而成,味道鲜美.牛肉汤的主料所含有的营养素没有包括的是( )
“淮南牛肉汤”是淮南小吃,选用沿淮黄牛肉、千张、豆饼、红薯粉丝、辣椒油等为主原料,配上香料、高汤等辅料制作而成,味道鲜美.牛肉汤的主料所含有的营养素没有包括的是( )| A. | 维生素 | B. | 糖类 | C. | 蛋白质 | D. | 油脂 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
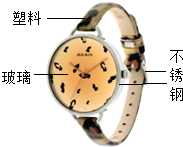 如图是中学生常佩戴的某款手表示意图:
如图是中学生常佩戴的某款手表示意图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com