
| A. | Mg和Ag | B. | Zn和Cu | C. | Al和Fe | D. | Al和Zn |
分析 这道题中,Mg、Zn、Al、Fe都是可以反应的,Ag、Cu都是不反应的.根据化学方程式计算即可正确选择.
解答 解:设要产生1g氢气,需要镁的质量为x,锌的质量为y,铝的质量为z,铁的质量为w,
Mg+2HCl═MgCl2+H2↑
24 2
x 1g
∴$\frac{24}{x}$=$\frac{2}{1g}$;
解之得:x=12g,
Zn+2HCl═ZnCl2+H2↑
65 2
y 1g
∴$\frac{65}{y}$=$\frac{2}{1g}$;
解之得:x=32.5g,
2Al+6HCl═2AlCl3+3H2↑
54 6
z 1g
∴$\frac{54}{z}$=$\frac{6}{1g}$,
解之得:z=9g;
Fe+2HCl═FeCl2+H2↑
56 2
w 1g
∴$\frac{56}{w}$=$\frac{2}{1g}$,
解之得:y=28g;
由以上计算可知,
A、镁为12g<15g,银不反应,可能;
B、锌为32.5g>15g,铜不反应,不可能;
C、铝为9g<15g,铁为28克>15克,可能;
D、铝为9g<15g,锌为32.5克>15克,可能;
故选B.
方法二:由于可与酸反应的金属,当制取1g氢气时,所需要的金属的质量=$\frac{金属的相对原子质量}{化合价}$,可知;生成1g氢气需要镁12g;锌需要32.5g;铝需要9g;铁需要28g.
A、生成1g氢气需要镁12g<15g,银不反应,可以平均出15g,故可能;
B、生成1g氢气需要锌32.5g>15g,铜不反应,不可以平均出15g,故不可能;
C、生成1g氢气需要铝9g<15g,铁为28克>15克,可以平均出15g,故可能;
D、生成1g氢气需要铝9g<15g,锌为32.5克>15克,可以平均出15g,故可能;
故选:B.
方法三:
假设金属的化合价都为+2价,设金属的平均原子质量x
Mg+2HCl═MgCl2+H2↑
x 2
15g 1g
∴$\frac{x}{15g}$=$\frac{2}{1g}$;
解之得:x=30.
由于是混合物,所以存在以下可能
1、两者都反应,则对应金属折算为+2价金属时,应该是相对原子质量一个大于30,一个小于30,因此C、D组合是可能的.
2、一个反应,一个不反应,则反应的金属必须折算为+2价时,相对原子质量小于30,则A也是可能的.
故选B.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


科目:初中化学 来源: 题型:解答题
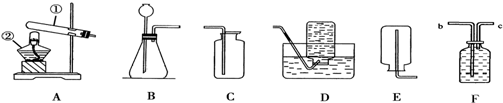
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 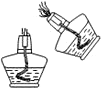 点燃酒精灯 | B. | 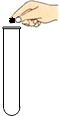 取用颗粒状固体 | C. |  量取液体体积 | D. | 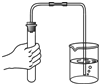 检查装置气密性 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com