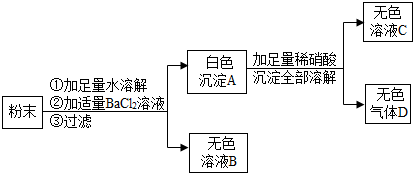
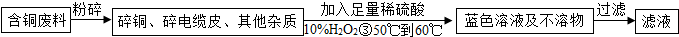(2012?润州区二模)在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组提出可以用含铜废料制备胆矾(CuSO
4?XH
2O).
查阅资料:(1)过氧化氢在常温下会缓慢分解为氧气和水.对其水溶液加热、光照或加催化剂(如MnO
2 )都会促进其分解.
(2)CuSO
4?XH
2O可溶于水,在加热时会生成CuSO
4和H
2O.
I、硫酸铜的制备
方案1:甲同学根据已学知识,提出了制备硫酸铜方案:

方案2:乙同学根据查阅资料找到了一种工业制备硫酸铜的流程:
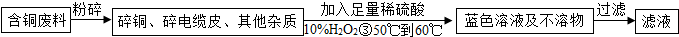
(1)写出上述方案中的②处铜或铜的化合物有关的化学反应方程式是:
CuO+H2SO4=CuSO4+H2O
CuO+H2SO4=CuSO4+H2O
.
(2)从环保角度对两套方案的不同部分进行比较,你认为方案
2
2
(填1或2)更合理.理由是:
耗能少或无污染
耗能少或无污染
.
(3)方案2中,加入H
2O
2后要求温度控制在50℃到60℃加热的可能的原因为
防止H2O2受热分解
防止H2O2受热分解
.
(4)若上述方案所用的稀硫酸是在实验室中由稀释浓硫酸得到,在稀释浓硫酸时的操作是:
将浓硫酸沿烧杯壁缓缓倒入水中
将浓硫酸沿烧杯壁缓缓倒入水中
并用玻璃棒不断搅拌
并用玻璃棒不断搅拌
.
(5)兴趣小组同学一致指出,将滤液经蒸发、降温结晶等操作后,用少量95%的酒精淋洗后晾干,得硫酸铜晶体.晶体采用酒精淋洗的优点是
减少硫酸铜晶体因溶于水而损失
减少硫酸铜晶体因溶于水而损失
.
II、硫酸铜晶体(CuSO
4?xH
2O)中结晶水(xH
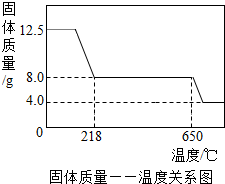
2O)含量的测定学习小组取12.5g硫酸铜晶体(CuSO
4?xH
2O)进行热分解,
获得相关数据,并绘制成固体质量一温度的关系如图.
(1)在加热过程中,随着水分的失去,固体颜色将由蓝色逐渐变为
白
白
色,最终变为黑色;
(2)650℃以上时,硫酸铜固体就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为
;
(3)根据图中数据,计算CuSO
4?xH
2O中x的值为
5
5
.(请写出计算过程)
(4)若将4.0g剩余固体继续加热到更高的温度,发现固体质量减少了0.4g后质量不再改变,写出剩余固体的化学式:
Cu2O
Cu2O
.
Ⅲ、硫酸铜的应用
波尔多液是用硫酸铜和石灰乳配成的一种天蓝色、粘稠的悬浊液,其有效成分是Cu
4(OH)
6SO
4,其中铜元素的化合价为
+2
+2
.碱式盐可以写成盐和碱的形式,例如碱式碳酸铜可以写成CuCO
3?Cu(OH)
2,则Cu
4(OH)
6SO
4可以写成盐和碱的形式为
CuSO4?3Cu(OH)2
CuSO4?3Cu(OH)2
,其杀菌机理可看作是Cu
2+使病原菌失去活性,这说明病原菌的主体是
蛋白质
蛋白质
(填一种有机物名称).