
分析 (1)由质量守恒定律计算出生成沉淀的质量,由恰好完全反应时生成沉淀的质量,根据反应的化学方程式,计算样品中氯化钙的质量,即可解答;
(2)当氯化钙与碳酸钠恰好完全反应时,过滤,所得溶液为氯化钠溶液,其中溶质氯化钠质量为样品中氯化钠与反应生成氯化钠的质量和,利用溶液中溶质的质量分数计算公式计算所得溶液中溶质的质量分数.
解答 解:(1)由质量守恒定律可得出生成沉淀的质量:20g+85g+103g-200g=8g
设样品中氯化钙的质量为x,生成氯化钠的质量为y
CaCl2+Na2CO3═CaCO3↓+2NaCl
111 100 117
x 8g y
$\frac{111}{x}$=$\frac{117}{y}$=$\frac{100}{8g}$
解得:x=8.88g y=9.36g
融雪剂中氯化钙的质量分数为:$\frac{8.88g}{20g}$×100%=44.4%.
(2)所得溶液的溶质质量分数为:$\frac{20g-8.88g+9.36g}{200g}$×100%=10.2%
答:(1)融雪剂中氯化钙的质量分数为44.4%.
(2)所得溶液的溶质质量分数为10.2%.
点评 主要考查学生对完全反应的认识,以及运用化学方程式和溶质质量分数公式进行计算的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


科目:初中化学 来源: 题型:选择题
| A. | 在铁板表面镀上一层锌成为白铁,白铁是铁锌合金 | |
| B. | 铁是地壳中含量最多的金属元素 | |
| C. | 炼铁高炉炼出来的是生铁不是钢 | |
| D. | 从高炉排出来的废气,可以直接放空气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
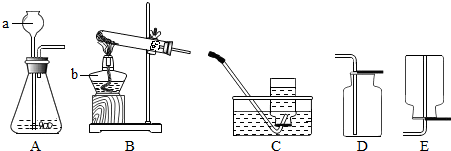
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 某化肥包装袋上的部分说明如图所示
某化肥包装袋上的部分说明如图所示查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HCl | B. | CuCl2 | C. | FeCl2 | D. | CuO |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
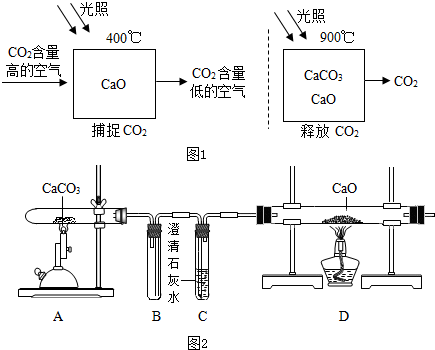
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量D中固体加入试管中,加水震荡,滴入无色酚酞试液, 再向试管中加入足量的稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅱ成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com