
分析 滤渣是二氧化锰的质量,根据二氧化锰的质量可以计算反应生成锰酸钾和氧气的质量,进一步可以计算所得滤液中溶质的质量分数.
解答 解:(1)设反应生成锰酸钾的质量为x,生成氧气的质量为y,
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
197 87 32
x 1.09g y
$\frac{197}{x}$=$\frac{87}{1.09g}$=$\frac{32}{y}$,
x=2.47g,y=0.40g,
答:生成了0.40g氧气.
(2)滤液质量为:3.95g+97.54g-1.09g-0.40g=100g,
所得滤液中溶质的质量分数为:$\frac{2.47g}{100g}$×100%=2.47%,
答:所得滤液中溶质的质量分数为2.47%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:选择题
| 主食 | 米饭 |
| 副食 | 红烧肉 清蒸鱼 炒蛋 |
| 饮料 | 牛奶 |
| A. | 鸡块 | B. | 大白菜 | C. | 糖醋排骨 | D. | 豆腐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D | |
| 体液 | 血浆 | 唾液 | 胃液 | 尿液 |
| pH | 7.35~7.45 | 6.6~7.1 | 0.9~1.5 | 4.7~8.4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
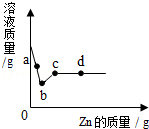 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn粉,溶液质量与加入Zn粉的质量关系如图所示.关于该实验有如下说法:
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn粉,溶液质量与加入Zn粉的质量关系如图所示.关于该实验有如下说法:| A. | 0个 | B. | 1个 | C. | 2个 | D. | 3个 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
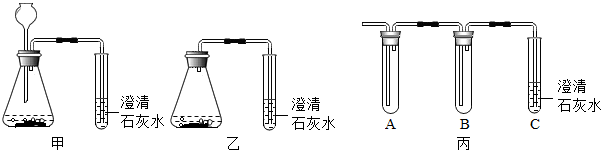
| 实验 | 实验步骤 | 实验现象 | 实验结论 |
| 实验Ⅰ | 将纯净的CO2通入到该实验所用的澄清石灰水中 | 澄清的石灰水边浑浊 | 猜想一不成立 |
| 实验Ⅱ | 将反应产生的气体通入到硝酸银溶液中 | 有白色沉淀产生 | 猜想二成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间(min) 浓度 催化剂 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| 加入WgMnO2 | 0.2 | 0.8 | 2.0 |
| 加入WgFe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 固体样品可能由三种物质组成 | B. | 固体样品是CuO与Cu2O的混合物 | ||
| C. | 固体样品可能是Cu2O | D. | 固体样品可能由CuO和Cu组成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com