
分析 根据过量的BaCl2能与Na2SO4反应生成硫酸钡沉淀和氯化钠,过量的Na2CO3溶液能与CaCl2、过量的氯化钡反应,分别生成碳酸钙沉淀和氯化钠、碳酸钡沉淀和氯化钠,结合过滤操作所需的仪器、质量守恒定律,进行分析解答.
解答 解:食盐水中含有杂质CaCl2和Na2SO4,依次加入过量的BaCl2和Na2CO3溶液后,过量的BaCl2能与Na2SO4反应生成硫酸钡沉淀和氯化钠,过量的Na2CO3溶液能与CaCl2、过量的氯化钡反应,分别生成碳酸钙沉淀和氯化钠、碳酸钡沉淀和氯化钠,过滤滤液中溶质为氯化钠和过量的碳酸钠.
过滤是把不溶于液体的固体与液体分离的一种方法,过滤操作的装置由铁架台、烧杯、玻璃棒、漏斗四种仪器组成,其中玻璃仪器有烧杯、玻璃棒和漏斗.
向食盐水中通NH3和CO2可制得小苏打和一种氮肥,由质量守恒定律,反应前后元素种类不变,则该氮肥为碳酸氢铵,其化学式为:NH4HCO3.
故答案为:氯化钠、碳酸钠;漏斗;NH4HCO3.
点评 本题难度不大,掌握盐的化学性质、过滤操作的原理与所需的仪器、质量守恒定律等是正确解答本题的关键.


科目:初中化学 来源: 题型:实验探究题
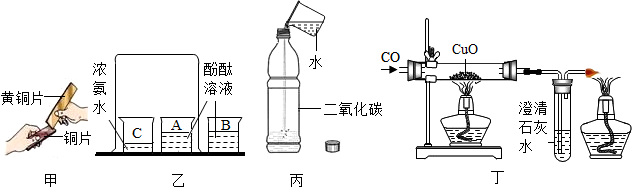
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | A | B | C | D |  |
| 微观示意图 |  | 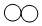 |  |  |
| A. | 该反应属于置换反应 | |
| B. | A、B、C、D的化学计量数之比为2:1:2:2 | |
| C. | 反应前后有元素的化合价发生改变 | |
| D. | 若有64 g B参加反应,则生成C的质量为64 g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将CO2通入深海海底要消耗大量能源,消耗能源也会加剧CO2的排放 | |
| B. | 海水呈弱碱性,大量CO2溶于海水生成碳酸,会使海水的酸性增大 | |
| C. | CO2是光合作用的原料,储存在海底,会使很多陆上植物的光合作用停止 | |
| D. | 当发生海底地震时,深海海底储存的CO2会被重新释放到大气中 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| NaCl | 35.7g | 36.0g | 36.6g | 37.3g | 38.4g |
| NH4Cl | 29.4g | 37.2g | 45.8g | 55.2g | 65.6g |
| A. | NaCl的溶解度比NH4Cl小 | |
| B. | 控制温度在0~20℃之间时,两种物质可配出质量分数相同的饱和溶液 | |
| C. | NaCl中含有少量NH4Cl时,可通过冷却热饱和溶液的方法来提纯NaCl | |
| D. | 80℃时将两种物质各5 g分别加入到10 g水中,固体均能全部溶解 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com