
以钛铁矿(主要成分为FeTiO3,同时含有少量的Fe2O3 、FeO等)为原料制TiO2,再由TiO2制金属Ti的工艺流程如下:
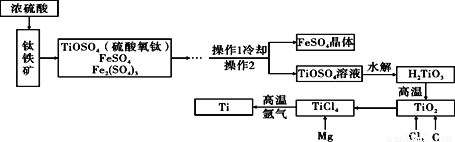
(1)写出由TiCl4制得Ti的化学反应方程式(已知该反应为置换反应): ___________。
(2)由H2TiO3制得TiO2的反应与碳酸分解类似,写出该反应方程式: ___________。
(3)工艺流程中,水解属于_________变化。(填“物理”或“化学”)
(4)操作2的名称是________________。
(5)TiO2可与焦炭、氯气在高温下反应,该反应为TiO2+2C+2Cl2==TiCl4+2X,则物质X的化学式为__________。
2Mg + TiCl4 2MgCl2 + Ti H2TiO3 H2O +TiO2 化学 过滤 CO 【解析】本题考查了化学变化和物理变化的判别,质量守恒定律及其应用,化学方程式的书写等。 (1)四氯化钛和镁在高温的条件下发生置换反应,生成钛和氯化镁,化学方程式为:2Mg + TiCl4 2MgCl2 + Ti; (2)钛酸分解生成二氧化钛和水,化学方程式为:H2TiO3 H2O ...科目:初中化学 来源:广东省汕头市金平区2018届九年级下学期教学质量监测化学试卷 题型:填空题
根据图中提供的信息,请回答下列问题:
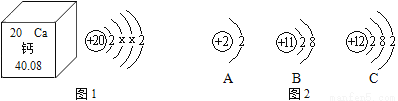
(1)由图1可知,钙的相对原子质量为________________,x=______________。
(2)图2中与钙元素化学性质相似的是________________;
(3)ABC中位于同周期的是____________________。
40.08 8 C BC 【解析】由题中信息指,(1)由图1可知,钙的相对原子质量为40.08,x=8。(2)图2中与钙元素化学性质相似的是C,最外层电子数决定元素的化学性质,钙元素最外层2个电子。(3)ABC中位于同周期的是BC,电子层数决定元素周期数,BC原子电子层数相同,属于同一周期。 点睛∶元素最外层电子数决定元素的化学性质,电子层数决定元素周期数。查看答案和解析>>
科目:初中化学 来源:湖南省邵阳市毕业学业模拟考试(二)化学试卷 题型:单选题
现有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲、乙表面有气泡产生,且甲产生气泡较快;再把丙和丁投入相同的硝酸银溶液中,过一会儿,丙的表面有银析出,而丁没变化。则四种金属的活动性顺序是( )
A.丙>乙>丁>甲
B.丁>乙>丙>甲
C.甲>乙>丙>丁
D.乙>甲>丁>丙
C 【解析】 试题分析:由题意可知,甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀硫酸中,只有甲、乙表面有气泡产生,且甲产生气泡较快,可推出甲的活泼性大于乙,且都大于丙、丁;由再把丙和丁投入相同的硝酸银溶液中,过一会儿,丙的表面有银析出,而丁没变化,说明了丙的活泼性大于丁。由此可得出甲、乙、丙、丁四种的金属的活泼性大小是:甲>乙>丙>丁。所以C正确,A、B、D错误。故选...查看答案和解析>>
科目:初中化学 来源:湖南省邵阳市毕业学业模拟考试(二)化学试卷 题型:单选题
构成物质的微粒有分子、原子、离子。下列物质由原子构成的是( )
A. 水 B. 氮气 C. 食盐 D. 氖气
D 【解析】A、水是非金属元素组成的化合物,由水分子构成的,错误;B、氮气属于气态非金属单质,是由氮分子构成的,错误;C、食盐(氯化钠的俗称)是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的,错误;D、氖气属于稀有气体单质,是由氖原子直接构成的,正确。故选D。查看答案和解析>>
科目:初中化学 来源:广东省广州市2018届中考一模化学试卷 题型:科学探究题
某兴趣小组在准备化学实验基本技能考试时,对以下问题进行了探究。
I.探究酸和碱能否发生化学反应
(1)方案l:甲同学向盛有少量NaOH溶液的试管中滴几滴无色酚酞试液,振荡,继续加入稀硫酸,观察到溶液由________色变成无色。甲同学得出结论:酸和碱能发生反应。
方案2:乙同学取少量NaOH溶液,测得溶液pH为10,向该溶液中加入一定量稀硫酸后,测得溶液pH为9,乙同学发现溶液pH减小了,得出结论:酸和碱能发生反应。
(2)交流讨论:大家同意甲同学的结论,对乙同学的实验过程提出质疑,溶液pH减小的原因还可能是稀硫酸中的水稀释了NaOH溶液;大家认为,乙同学向NaOH溶液中加入稀硫酸后,测得溶液的pH必须________7(填“大于”、“小于”或“等于”),才能证明酸和碱能发生反应。
II.探究酸和碱反应后溶液中溶质的成分
丙同学对探究I中甲同学实验后的无色溶液展开探究。
【提出问题】试管中无色溶液的溶质除了酚酞还有什么?
【提出猜想】猜想(l):Na2SO4;猜想(2):Na2SO4和____________。
【设计实验】现实验室提供以下试剂:锌粒、铜片、氯化钡溶液、氢氧化钠溶液以及必要的实验仪器,请完成下列表格:
实验操作 | 实验现象 | 实验结论 |
_____________ | _________ | 猜想(2)成立 |
【实验结论】猜想(2)成立
红 等于或小于 H2SO4 取适量甲同学实验反应后的溶液于试管中,加入锌粒,观察现象 锌粒溶解,并有气泡产生 【解析】本题考查了中和反应,酸、碱的化学性质。 Ⅰ、方案l:氢氧化钠溶液显碱性,滴入无色酚酞试液变红色,继续加入稀硫酸,硫酸与氢氧化钠发生中和反应生成硫酸钠和水,当加入的硫酸将氢氧化钠完全中和后,溶液变成无色,得出结论:酸和碱能发生反应; 方案2:溶液pH减小的原因还可能...查看答案和解析>>
科目:初中化学 来源:广东省广州市2018届中考一模化学试卷 题型:单选题
下列图像能正确反映其对应操作的是

A. A B. B C. C D. D
C 【解析】A、向一定量的NaOH溶液中逐滴加入稀盐酸,氢氧化钠与盐酸发生中和反应生成氯化钠和水,氯化钠的质量从无到有,逐渐增大,溶液中氯化钠的质量分数增大,当氢氧化钠被完全中和后,氯化钠的质量不再增大,溶液中氯化钠的质量分数达到了最大值,但是随着继续滴加稀盐酸时溶液的质量增大,氯化钠的质量不变,溶液中氯化钠的质量分数会减小,图中所示与事实不符,错误;B、足量的金属与酸反应,由于氢气中氢元素...查看答案和解析>>
科目:初中化学 来源:广东省广州市2018届中考一模化学试卷 题型:单选题
下列说法不正确的是
A. 饱和溶液的质量分数一定大于不饱和溶液
B. 硝酸铵固体在溶解时会出现吸热现象
C. 酒精、汽油、水都可以做溶剂
D. 酸和碱发生中和反应生成盐和水
A 【解析】A、没有指明温度,无法比较饱和溶液与不饱和溶液的质量分数,错误;B、硝酸铵固体溶于水吸热,使溶液的温度降低,正确;C、酒精、汽油、水都是常见的溶剂,都可以做溶剂,正确;D、中和反应是酸与碱作用生成盐和水的反应,酸和碱发生中和反应生成盐和水,正确。故选A。查看答案和解析>>
科目:初中化学 来源:江苏省常州市武进区2018届九年级第一次模拟考试化学试卷 题型:科学探究题
某研究小组对H2O2分解的各种催化剂的催化效果进行定量对比探究。小组人员选用海藻酸钠(海藻酸钠是一种天然高分子物质,在本实验中性质稳定)作为催化剂支架,制备负载不同催化剂的海藻酸钠微球,利用数字化手持技术展开探究。
【实验过程】 取负载各种催化剂的海藻酸钠微球各30粒分别放入4个锥形瓶中,连接压力传感器(如图1所示)。用注射器分别向每个锥形瓶中注入20 mL浓度为5% H2O2溶液,溶液全部注入瞬间立即采集200 s内压强数据,最后用软件绘制实验图形如图2所示(肝脏研磨液富含过氧化氢酶,酶主要成分为蛋白质)。 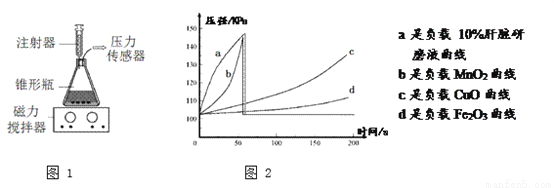
【实验分析】
⑴ 写出b瓶中反应的化学方程式____。上述四种中催化效果最差的物质是___。
⑵ a、b、c瓶中的海藻酸钠微球都浮了起来,主要原因是_______。
⑶ a 、b瓶在60秒左右时压强突然恢复到常压,最可能原因是_____。
⑷ 前50秒内,b、c、d瓶中反应速率越来越快,可能原因是_____,实验中发现a瓶中催化剂的性能随反应进行越来越弱,可能原因是:__________。
⑸ 若实验中过氧化氢溶液完全反应,则本实验理论上每瓶能得到氧气的质量为多少__________?(5%的过氧化氢溶液密度约为1g/mL,最终结果精确到小数点后两位)
2H2O2 2H2O+ O2↑ Fe2O3 产生的大量气体附着在小球表面,浮力变大。 瓶内压强太大导致冲塞(或注射器活塞飞出) 反应放热 温度升高部分蛋白质失去生理活性(酶的活性降低) 0.47g。 【解析】根据所学知识和题中信息知,探究H2O2分解的各种催化剂的催化效果。【实验过程】取负载各种催化剂的海藻酸钠微球各30粒分别放入4个锥形瓶中,用注射器分别向每个锥形瓶中注入20 mL浓度为5...查看答案和解析>>
科目:初中化学 来源:广东省佛山市顺德区2018届九年级教学质量检测化学试卷 题型:单选题
下图为硒元素在周期表中的信息及其原子结构示意图,对该元素的认识正确的是

A. m的值为8
B. 是一种金属元素
C. 相对原子质量为78.96 g
D. 与氢元素能形成化学式为H2Se的化合物
D 【解析】A、根据元素在元素周期表中的信息及质子数=核外电子数可知,X=2+8+m+6=34,则m=18,错误;B、硒带“石”字旁,是一种非金属元素,错误;C、由元素在元素周期表中的信息可知,硒的相对原子质量为78.96,错误;D、硒的原子结构中最外层电子数为6,容易得到2个电子,带2个单位负电荷,显-2价,H通常显+1价,与氢元素能形成化学式为H2Se的化合物,正确。故选D。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com