
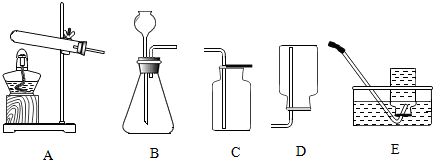
分析 (1)实验室要用KClO3和MnO2制取氧气,属于固体加热型制取气体,据此结合实验室制取氧气的注意事项,进行分析解答.
(2)根据氧气的密度比空气的大,结合氧气验满的方法,进行分析解答.
解答 解:(1)实验室要用KClO3和MnO2制取氧气,属于固体加热型制取气体,应选用发生装置是A.
用排水法收集氧气结束时,先把导管移出水面,再熄灭酒精灯,以防止水槽中的水倒吸入试管,使试管因骤然冷却而炸裂.
(2)氧气的密度比空气的大,装满氧气的集气瓶应盖上玻璃片后,应正放在桌面上;检验氧气是否收集满时,应将带火星的木条放在集气瓶口,若木条复燃,证明集满了氧气.
故答案为:(1)A;把导管移出水面;(2)正放;将带火星的木条放在集气瓶口,观察木条是否复燃.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取氧气的反应原理、发生装置和收集装置的选择依据是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | FeCl3、CuSO4、NaCl | B. | BaCl2、Na2SO4、NaOH | ||
| C. | CaCl2、NaNO3、AgNO3 | D. | K2SO4、NaNO3、NH4Cl |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
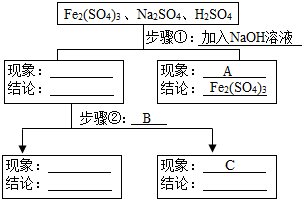 某同学设计鉴别物质引导图图下:
某同学设计鉴别物质引导图图下:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 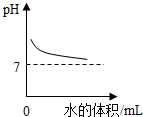 氢氧化钠溶液加水稀释 | |
| B. | 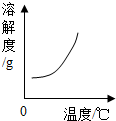 一定压强下,氧气在水中的溶解度 | |
| C. | 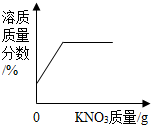 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | |
| D. | 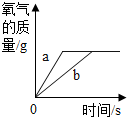 氯酸钾和二氧化锰混合加热制氧气中,a使用催化剂,b未使用催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
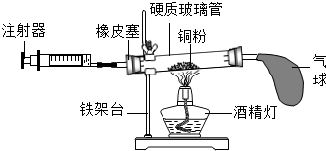
| A. | 铜粉用量的多少,不会影响实验结果 | |
| B. | 实验结束后冷却到室温才能读数 | |
| C. | 气球的作用是调节气压,使氧气完全反应 | |
| D. | 在正常操作情况下,反应结束后消耗氧气的总体积应该是反应前注射器内气体体积的$\frac{1}{5}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液质量分数 | B. | 溶液的pH | ||
| C. | 氢氧化钠的溶解度 | D. | 最多能吸收二氧化碳的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
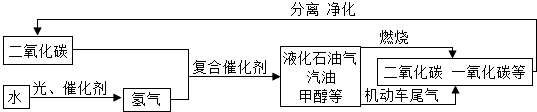
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
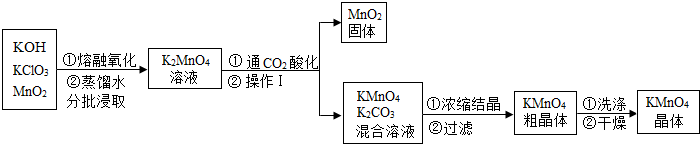
| 物质 | K2CO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 11.1 | 6.34 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com