
【题目】近来有科学家提出采用“碳捕捉”技术将CO和CO2 混合气体中的CO2 捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出)。则回答:
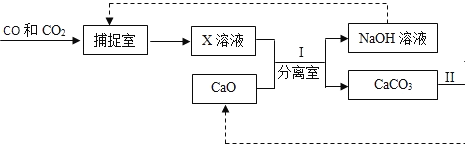
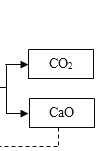
(1)反应②分离出的CO2可制成干冰,干冰常用于________;
(2)反应①在“反应分离室”内进行,将NaOH溶液与CaCO3分离的操作是______;
(3)“捕捉室”中发生反应的化学方程式是____________________;
(4)下列有关该捕捉过程的叙述正确的有(__________)
A 捕捉到的CO2 可制备其他化工产品,减少了温室气体的排放
B “反应分离室”中的反应要吸收大量的热
C 整个过程中,只有一种物质可循环使用
D 能耗大是该捕捉技术的一大缺点
【答案】人工降雨、食品冷藏等 过滤 CO2+2NaOH=Na2CO3+H2O AD
【解析】
(1)反应②分离出的CO2可制成干冰,干冰即固体二氧化碳,易升华吸热,常用于人工降雨、食品冷藏、制造舞台云雾效果等;
(2)反应①在“反应分离室”内进行,将NaOH溶液与CaCO3分离,即将不溶于水的固体与液体分离,操作是过滤;
(3)“捕捉室”中,一氧化碳不反应,二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式是CO2+2NaOH=Na2CO3+H2O;
(4)A、捕捉到的CO2 可制备其他化工产品,减少了二氧化碳(温室气体)的排放,故可减少温室气体的排放,选项正确;
B、“反应分离室”中的反应是氧化钙和水反应生成氢氧化钙,该反应放出大量的热,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,该反应在常温下即可进行,所以反应分离室中的反应不需要吸收大量的热,选项错误;
C、整个过程中,二氧化碳、氢氧化钠都既是反应物,也是生成物,都可循环利用,选项错误;
D、该过程中,碳酸钙分解需要在高温条件下进行,故能耗大是该捕捉技术的一大缺点,选项正确。
故选AD。


科目:初中化学 来源: 题型:
【题目】人类生产、生活离不开化学。
(1)净化水的操作有①过滤②蒸馏③静置沉淀等多种,其中净化程度最高的操作是____(填序号)。净水器中经常使用活性炭,主要利用活性炭的____________性。
(2)实验时要处处注意安全。用完酒精灯后,必须用灯帽盖灭,熄灭火焰的主要原理是_____(填序号)。
A 降温到着火点以下 B 隔绝空气 C 清除可燃物
(3)打开汽水瓶盖,有气泡冒出,说明气体溶解度随压强减小而__________。
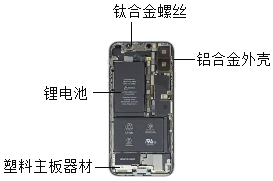
(4)如图是某电子产品拆解图片。图中标示的材料属于有机合成材料的是_________;选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度_________(填“大”或“小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合图示回答下列问题。
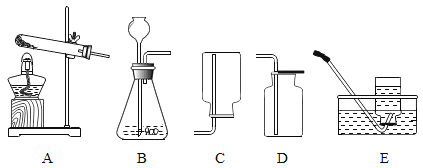
(1)上列图示各仪器中,金属仪器的名称是_____。
(2)实验室常用氯酸钾和二氧化锰固体混合制取氧气,发生反应的化学方程式为_____,上图中可以选用的发生装置是_____(填序号),如果选择E作收集氧气的装置,则当气泡_____时开始收集。
(3)若用过氧化氢溶液制取氧气,则可以选用的制取装置是_____(填序号),其反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钔是一种重要的金属元素,在元素周期表中的相关信息如下图所示。下列有关说法正确的是( )
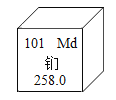
A.钔元素的原子核外有 157 个电子
B.钔单质的化学式为 Md
C.钔在化学反应中易得电子
D.钔的相对原子质量为 258.0g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某工厂处理废水中含有少量 FeCl3 的工艺流程,请根据题意回答下列问题:
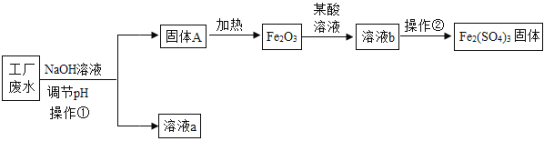
(1)操作①的名称是_____________;废水与氢氧化钠溶液反应属于___________(填反应类型)。
(2)加热固体 A 的化学方程式为______________________________。
(3)操作②过程中当__________________________即停止加热,其中玻璃棒的主要作用是__________。
(4)写出 Fe2O3 的一种工业用途__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁是四个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
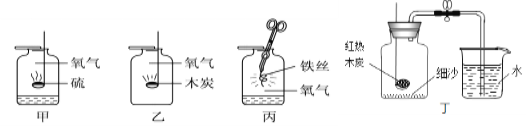
(1)依据丙实验回答:
①小明实验前将铁丝绕成螺旋状的目的是_____。
②铁丝在氧气中燃烧的文字表达式 _____。
(2)甲、丙两实验集气瓶中均放少量水,甲中加入少量水的目的是_____,丙中加入少量水的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的溶解度曲线,下列说法中正确的是( )
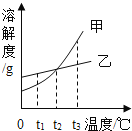
A.甲物质的溶解度小于乙物质的溶解度
B.t2℃时,甲物质的溶液和乙物质的溶液中含有溶质的质量相等
C.将t2℃时甲、乙两物质的饱和溶液升温至t3℃,所得甲、乙溶液中溶质的质量分数不相等
D.当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中可用煮沸的方法降低水的硬度,该过程中溶解的碳酸氢钙Ca(HCO3)2分解生成一氧化碳、水和一种盐,有关反应的化学方程式为______;向一定量的稀盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液,反应现象为______ 。若生成气体的质量是沉淀质量的4.4倍,则原混合液体中氯化氢和氯化钙的质量比为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某同学为配制10%的食盐溶液操作示意图。请据图回答:
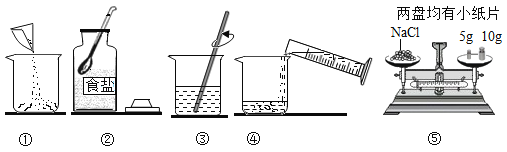
(1)称量食盐时,天平平衡时的状态如图⑤所示,游码标尺刚好位于零刻度线处,则配得的溶液质量为_____g;需要水的体积为_____mL;
(2)配制溶液的步骤为②→_____→③(用序号表示)。
(3)下列情况中,会使食盐溶液质量分数低于10%的是_____。
A 称取的食盐不纯,有杂质
B 在量取水时,俯视液面读数
C 配制好的溶液转移时,不小心有少量液体溅出
D 配制好的溶液装入刚清洗完还未干燥的试剂瓶保存
(4)溶解时,用玻璃棒搅拌的目的是 __________
(5)若要将40g 10%的氯化钠溶液浓度变为20%,需要蒸发_____g的水。
(6)将100g10%的某固体物质M的溶液,分别进行下述操作,所得溶液中溶质的质量分数最小的是____
A 蒸发掉10g水,无晶体析出 B 加入10g10%的M的溶液
C 加入10g固体M,并使之完全溶解 D 加入10g水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com