
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
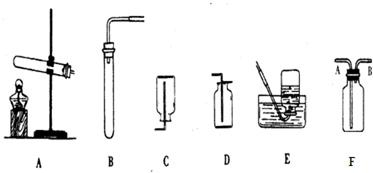 27、化学实验室里,老师给同学们准备了如下实验装置:
27、化学实验室里,老师给同学们准备了如下实验装置:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 溶度 时间(S) 反应条件 |
30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化、不加热 | 10 | 25 | 60 | 120 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
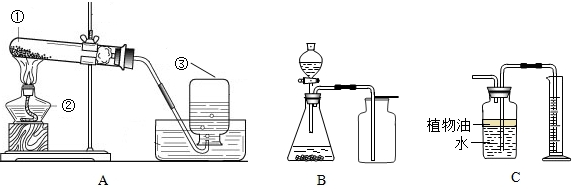
| 加热 |
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 木条不复燃 | 常温下过氧化氢溶液分解速度慢 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com