
| 装置编号 | 加入水的体积 | 加入水的温度 | 收集到的气体的体积 |
| 1 | 200mL | 15℃ | a(待记录) |
| 2 | 200mL | 50℃ | b(待记录) |
分析 根据质量守恒定律化学反应前后元素的种类和原子的个数不变推断物质的化学式;根据物质的性质确定其检验方法;设计实验时要注意控制变量;根据气体在水中的溶解度与温度有关进行分析解答即可.
解答 解:【实验一】(1)3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3X↑,反应前含有3个Na原子,11个H原子,9个C原子,16个O原子,反应后含有3个Na原子,11个H原子,6个C原子,10个O原子,故3X中含有3个C原子,6个O原子,故X中含有1个C原子,2个O原子,故其化学式为CO2;检验二氧化碳使用的是澄清的石灰水,故填:CO2;澄清石灰水;
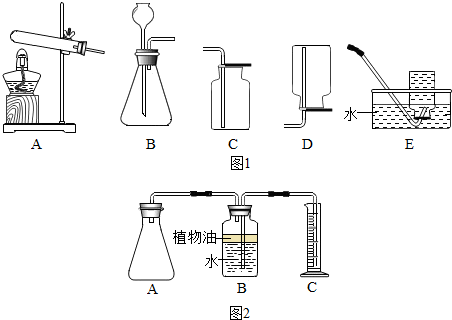
(2)实验室以柠檬酸和小苏打粉末混合后加水反应制取二氧化碳,则选用的发生装置是B,二氧化碳能溶于水密度大于空气,故收集装置是C,故填:B;C;
【实验二】(1)设计实验要注意控制变量,故水的体积是200mL,故填:200 mL;
(2)由于二氧化碳能溶于水,故可以加油层,防止二氧化碳溶解,故填:防止二氧化碳溶解在B装置的水中;
(3)根据实验1和实验的比较可以看出,二者的温度不同,故“汽泡爽”产生气体的量与加水温度有关系,故填:“汽泡爽”产生气体的量与加水温度有关系;
实验2温度高,收集到的气体的体积较大,而实验1温度较低,收集的气体的体积较小,说明温度高气体在水中的溶解度小,收集到的气体多,故填:温度高气体在水中的溶解度小,收集到的气体多;
(4)要证明是温度高气体溶解的小,可以将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积,故填:将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
点评 本题考查的是常见物质的性质以及影响气体溶解的因素的实验探究,完成此题,可以依据已有的知识进行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
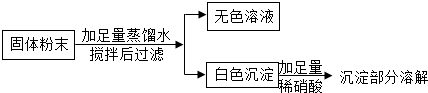
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
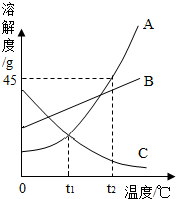 如图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 剧烈燃烧,大量火星 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验编号 | 活性炭纯度 | 活性炭的用量(克) | 消失时间(秒) |
| 1 | 80% | 1.0 | 60 |
| 2 | 9.0 | 45 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 实验步骤 | 预期现象 | 结论 |
| 方案1 | 取样,滴入适量的硝酸钡溶液 | 出现白色沉淀 | 有硫酸 |
| 方案2 | 取样,滴入盛有锌粒的试管中 | 出现气泡 | 有硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
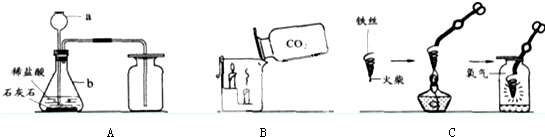
 某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.| 实验操作 | 实验现象 | 结论及反应的方程式 |
| 从烧瓶内取少量反应后的澄清溶液分别于两支试管中,分别滴加澄清石灰水、碳酸钠溶液 | 加入二者后均无明显现象 | 我的猜想正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com