
【题目】根据下列实验装置图,回答问题:
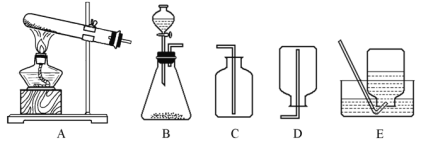
(1)在B装置中,由无机材料制成的仪器是____(写一种即可)。
(2)收集某气体只能用C装置,说明该气体具有____、____等物理性质。
(3)实验室用AE装置制取氧气,有关的化学方程式是____;气体收集完毕,接下来的先、后操作是____。
(4)实验室常用金属锌与稀硫酸反应制取氢气,该反应的基本类型是____反应;要得到高纯度的氢气,应选择的装置组合是____。
【答案】分液漏斗(或锥形瓶) 易溶于水 密度比空气大 ![]() 先将导管移出水面,再熄灭酒精灯 置换 BE
先将导管移出水面,再熄灭酒精灯 置换 BE
【解析】
(1)在B装置中,锥形瓶或分液漏斗都是无机非金属材料,由无机材料制成的仪器是锥形瓶或分液漏斗;
(2)实验室收集某气体只能用C装置,说明该气体只能用向上排空气法收集,不能用排水法收集,该气体的密度大于空气、易溶于水;
(3)实验室用AE装置制取氧气,发生装置是固体加热型,由于试管口没有棉花,所以是用加热氯酸钾和二氧化锰混合物的方法来制取氧气,氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,反应的化学方程式为:![]() ;为防止水倒流引起试管的炸裂,气体收集完毕,接下来的先、后操作是先将导管移出水面,再熄灭酒精灯;
;为防止水倒流引起试管的炸裂,气体收集完毕,接下来的先、后操作是先将导管移出水面,再熄灭酒精灯;
(4)实验室常用金属锌与稀硫酸反应制取氢气,锌与硫酸反应生成硫酸锌和氢气,该反应由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应,基本类型是置换反应;金属锌与稀硫酸反应制取氢气,反应物是固体和液体,不需加热,氢气难溶于水,可用排水法收集,要得到高纯度的氢气,应选择的装置组合是BE。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法中不正确的是( )
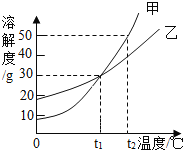
A. 当温度大于t1℃时,同温比较溶解度:甲物质>乙物质
B. t1℃时,甲和乙的饱和溶液中溶质的质量分数相等
C. t1℃时,甲饱和溶液中溶质质量分数为30%
D. 甲的饱和溶液从t2℃降温到t1℃,还是饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】飞机C919是我国自行研制的,标志着我国飞机制造技术的飞跃。请回答:
(1)利用CO还原赤铁矿石可制得铁单质,其反应的化学方程式为___。
(2)飞机上的螺丝钉一般不用铁质的,其原因是铁易与___反应而生锈。
(3)铝比铁活泼,但铝制品耐腐蚀的原因是___。
(4)飞机的厨房为乘客提供了以下食物:快餐、雪碧、牛奶、蔬菜面条等。蔬菜面条比普通面条多提供的营养物质主要是___。
(5)飞机急救箱中备有消毒剂过氧化氢溶液,过氧化氢中氧元素的化合价为___。
(6)飞机上的座椅套采用耐磨耐腐蚀的“尼龙”,它属于___材料。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】课堂上老师对探究干电池原理的实验进行如下改进,图甲:把一块锌片和一根碳棒同时插入盛有稀硫酸的U型管中;图乙:用导线将锌片和碳棒连接起来插入盛有稀硫酸的U型管中,并在导线中间连接一只灵敏电流计。
请按要求回答相关问题
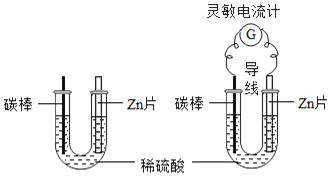
甲 乙
(1)图乙主要的能量转化形式是_______。
(2)乙观察到与甲不同的现象是_______。
(3)配制所需稀硫酸:现有98%的浓硫酸18g(体积为9.8mL),可将其配成24.5%的硫酸溶液_______g,配制的具体操作过程是_______(水的密度为1g/mL)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料在国民生产和日常生活中得到普遍广泛的应用
(1)用如图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁片);
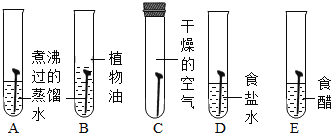
①甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,认为必须全面观察试管_______(选填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论。B中植物油的作用是_______。
②试管D和E实验的目的是进一步探究铁在_______的环境中是否更容易锈蚀。
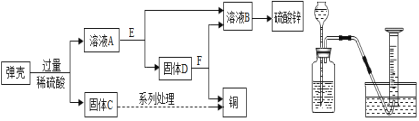
(2)黄铜(铜锌合金)用作弹壳的制造。现有一批使用过的,锈迹斑斑的弹壳,处理这批弹壳可以制得硫酸锌和铜,其主要流程如图甲所示:
(收集资料)弹壳上的锈主要为Cu2(OH)2CO3,能与稀硫酸反应得到硫酸铜溶液;弹壳中其他杂质不溶于水,也不参加反应。
甲 乙
①写出弹壳上的锈与稀硫酸反应的化学方程式_______。
②固体D为_______。从微观的角度来看,A与E的反应微观实质是_______。
(3)为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小昊设计了一套实验装置(如图乙),他取两种金属各m克,分别加入足量的稀硫酸进行反应,在相同条件下测定不同时间内收集到的气体体积,实验记录如表:
反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 | |
收集到的气体体积(毫升) | 甲金属 | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
乙金属 | 30 | 75 | 120 | 150 | 150 | 150 | 150 | |
①由实验结果可知:金属活动性较强的是_______。实验中,除了要控制两种金属的质量相等,还需要控制的变量有_______。
②为了使得到的实验数据准确,小昊开始收集气体的时间点应该是_______(填字母)
A.导管口一有气泡冒出时 B.冒出气泡连续且均匀时C.检验产生的气体纯净时
③根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道的数据是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小红利用氧气、二氧化碳传感器在装有两支燃着的高低蜡烛的密闭容器内顶部测容器内两支蜡烛从点燃到全部熄灭后,氧气(上)和二氧化碳(下)的浓度变化,如图所示。最终剩余氧气浓度15.65%,CO2浓度1.89%.则下列说法不正确的是( )

A. 支持蜡烛燃烧的氧气浓度须达到21%
B. 点B时两支蜡烛全部熄灭
C. 曲线BC段因为蜡烛熄灭,温度下降,二氧化碳密度大下沉,氧气上浮
D. 容器内高的蜡烛先熄灭矮的蜡烛后熄灭
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法正确的是( )
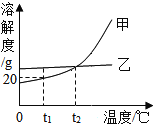
A. 甲的溶解度比乙大
B. t2℃时,甲、乙的饱和溶液中溶质的质量相等
C. t1℃时,在50g水中加入15g甲,可得到 65g 溶液
D. 要使接近饱和的甲溶液转化为饱和溶液,可采用降温的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“科技是第一生产力”,我国科学家在科技发展道路上做出了突出的贡献。
(1)南仁东—— FAST 工程首席科学家、总工程师,被称为“天眼之父”。被誉为“中国天眼”的 FAST,是目前世界上最大单口径、最灵敏的射电望远镜,2016 年 9 月在贵州落成。如图所示,请回答下列问题:

①“ 中国天眼” 的“ 眼眶” 及塔架都是采用角钢制成, 角钢属于__________(填“无机非金属材料”“金属材料”“有机合成材料”之一)。
②角钢中含有锰(Mn)和硅,锰可以与稀盐酸发生置换反应,生成锰的化合物中锰元素显+2 价。请写出锰与稀盐酸反应的化学方程式:_____。
③铝有很好的抗腐蚀性,是因为铝在空气中易与氧气反应生成致密的_____(填化学式)薄膜。
(2)侯德榜——侯氏制碱法创始人,该方法就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠。碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题:
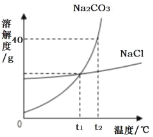
①t2℃时 Na2CO3 的溶解度_____NaCl 的溶解度(填“大于”“小于”“等于”之一) ;
②若 Na2CO3 中混有少量的 NaCl, 提纯 Na2CO3, 最好采取的方法是__________(填“降温结晶”或“蒸发结晶”)。
③将 t1℃时 NaCl 和 Na2CO3 的饱和溶液(溶液内均无固体剩余),均升温到 t2℃,所得 NaCl 溶液的溶质质量分数_____Na2CO3 溶液的溶质质量分数(填“大于”“小于”“等于”之一) ;
④t2℃时将 40g Na2CO3 固体加入 50g 水中,所得 Na2CO3 溶液中溶质与溶剂的质量比为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国制碱工业的先驱候德榜发明了“侯氏制碱法”,其生产过程涉及的主要化学反应如下:
①![]()
②![]()
③![]()
计算:
(1)反应①中X的化学式为_____
(2)工业纯碱中含有氯化钠,取55g工业纯碱,向其中加入269.5g稀盐酸,恰好完全反应,生成22g二氧化碳,求:
①工业纯碱中碳酸钠的质量:_____
②反应后溶液中溶质的质量分数。_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com