

���� ��1��������������ƣ�
��2�����ݻ�ѧ����ʽ���м��㡢���ݼ�����ˮ���ɵķ�����������
��3�����ݻ�ѧ��Ӧ��ԭ���Լ�������ܶ���������
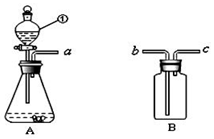
��� �⣺��1������������ƿ�������ƿ��
��2��������Ҫ������ص�����Ϊx����
2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2��
316 32
x 0.64g
$\frac{316}{32}=\frac{x}{0.64g}$
x=6.32g
���6.32��
��������ˮ���ռ����������ˮ����������ȷ����Ӧ���ˮ������ȼ�����ɡ����DZ������еģ���Ӱ��������ɵ���֤��Ϊ�ų�ˮ�����ĸ��ţ������ſ������ռ����������ܶȱȿ������������ſ����ռ��������ˮ���������Ԫ�ص���֤��
��3�������������ϡ���ᷴӦ�������������������������ܶȱȿ�����������װ��F�ռ���������ʱ������ӳ��ܽ��룻���FeS+H2SO4=FeSO4+H2S����a��
���� �˽�ʵ������ȡ����ķ�Ӧԭ��������װ�ã����ܽ�����ط���ʽ���㣬��ʵ�����ݽ�����ȷ�ķ����ͽ�𣬿�����ѧ����֪ʶ�����պ�Ӧ��������


 ��ʦ������Ԫ��ĩ���100��ϵ�д�
��ʦ������Ԫ��ĩ���100��ϵ�д� ��У������Ԫͬ��ѵ��������ϵ�д�
��У������Ԫͬ��ѵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ������������ | B�� | �������ϡ�������ˮ�� | ||
| C�� | ��Ȫˮ��ʳ�ס�ϡ������ | D�� | �Ά�Ŀ�����������̼��Һ̬�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������Ԫ�غ���Ԫ�ص�����֮����1��1 | |
| B�� | ������������ѧʽΪC4H8O2����̼���⡢��ԭ�ӵĸ���֮��Ϊ2��4��1 | |
| C�� | ����ͪ����ѧʽΪC4H6O2����̼Ԫ�ص�����������ߣ���Ԫ�ص������������ | |
| D�� | ��ϩ��C2H4������Ȳ��C2H2����ɵĻ������̼Ԫ��������������Ϊ93% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����0��y��8����ش�
����0��y��8����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ܺ���Mg2+ | B�� | һ������Cu2+ | ||
| C�� | һ������Cu2+ | D�� | һ������Fe2+��Mg2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
 �������ȡ���ռ��dz��л�ѧ�ĺ���֪ʶ��С��ͬѧ��ʵ���ҽ���������ȡ��̽��������һͬ���룺
�������ȡ���ռ��dz��л�ѧ�ĺ���֪ʶ��С��ͬѧ��ʵ���ҽ���������ȡ��̽��������һͬ���룺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ܶ�Խ��Խ�� | B�� | ����ѹǿ��С | ||
| C�� | ˮ�ķе����� | D�� | �����е�������ϡ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com