
��9����ʵ������һƿ������Һ����ʦ��С��ͬѧ��Ʒ����ⶨ�÷�Һ�����������������С��ͬѧ��ȡһ�ྻС�ձ�����������Ϊ18.2g��Ȼ�������е������������Һ�������������Ϊ33.2g��֮��һö����Ϊ10.8g������������ɰֽ��ĥȥ�����⣩�����С�ձ��з�Ӧ�����������治�������ݲ������ٴγ�����������Ϊ43.9 g��
��ش��������⣺
��1����Ӧ�в���������������� ��
��2������÷�Һ�����������������д��������̣�����������һλС��������6����
��3���������������δ�������Լ�������Ӱ���� (ѡ�ƫ����ƫС��������Ӱ�족)��ԭ���� ��
��1��0.1g ��2��32.7% ��3��ƫС�����������ⷴӦ
��������
��������������������غ㶨�ɣ���������������Ϊ��33.2g+10.8g-43.9g= 0.1g
(2)(6��) �������Һ��H2SO4����Ϊx
Fe + H2SO4 �� FeSO4 + H2��
98 2
X 0.1g
98/X=2/0.1g
x=4.9 g
��Һ��������������� ��4.9g/(33.2g-18.2g)*100% ��32.7��
���������������δ�������Լ�������Ӱ����ƫС,��Ϊ���������ⷴӦ������ɸ�����������������������ƫ�٣��̶���ɷ�Һ���������������ļ���ƫС��
���㣺�����غ㶨�ɡ��йػ�ѧ����ʽ�ļ��㡢�������������ļ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ�麣���п�һģ��ѧ�Ծ��������棩 ���ͣ������
��11�֣����Ա�ʵ�顱�ǻ�ѧѧϰ����֮��Ч��˼ά������ij��ѧѧϰС���ͬѧ��ѧ����صĻ�ѧ֪ʶ���߽�ʵ������������ʵ�飬������벢�ش��������⡣
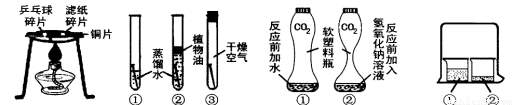
A B C D
A��ȼ�յ����� B�� �������������
C�� ֤��CO2��NaOH��Ӧ D�� �����˶�������
��1��ͨ��ʵ��A������˵��ȼ�յ�����֮һ�� ��ʵ����ʹ��ͭƬ����������ͭ�� �ԣ���һ���������ʣ�
��2������ʵ��B��һ��ʱ���۲쵽�Թ����е�����������ʴ���ɴ˵ó������������Ҫ���������� ֱ�ӽӴ�������ȥ������� ϴ�ķ�����
��3��ʵ��C�Ǹ�������ƿ���ij̶�֤��CO2 ��NaOH��Һ�е�����ȷʵ�����˷�Ӧ����ƿ������������ ����һ��Ӧ�Ļ�ѧ����ʽΪ ��
��4��ʵ��D���ձ����г��ֵ�������˵�������Dz����˶��ġ����ձ�����Һ����Ũ���ᣬ�ձ�����Һ���ǵ��з�̪��NaOH��Һʱ��һ��ʱ�����Һ��ɫ�ı仯�� ������������NaOH��Ӧ�Ļ�ѧ����ʽΪ ������ ��Ӧ���Ӧ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ�����б�ҵ��ѧҵˮƽ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ѧϰ��ѧ�ķ���֮һ�����������У������ε���
A���������� B������ C������þ D���Ȼ�þ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ��ͷ���������п�ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��ȥ���������е�����������ѡ�õ��Լ�����ȷ����( )
ѡ�� | ���� | �������� | ��ѡ���Լ��� |
A | NaOH��Һ | Na2CO3��Һ | ϡ���� |
B | CaO | CaCO3 | �������� |
C | CO2 | CO | ��ȼ |
D | ϡ���� | ϡ���� | ������Ba(NO3)2��Һ���ٹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ��ͷ���������п�ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������ȷ����( )

A���μ�Һ�� B��ȡ�ù��� C������ҺpH ���� D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ��ͷ�н�ƽ���п�ģ�⻯ѧ�Ծ��������棩 ���ͣ������
��7�֣���֪A���ᣬ��Ũ��Һ����ˮ�ԣ�BΪ���ʣ�CΪ�طʣ�
DΪ��ɫ������ˮ�Ĺ��塣����֮���ת����ϵ����ͼ��
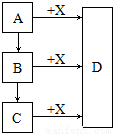
��1��D�������� ��
��2��A��X��Ӧ�Ļ�ѧ����ʽΪ�� ��
��3��Bת��ΪC�Ļ�ѧ����ʽΪ�� ��
��4��ʵ����ϡ��A��Ũ��Һ����������
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ��ͷ�н�ƽ���п�ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
С���ij��ɫ��Һ�������ʵļ�¼����������
A��HCl��NaOH��NaCl B��KNO3��NaCl��FeCl3
C��NaOH��Na2CO3��NaCl D��CuSO4��H2SO4��NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ��ͷ�б�ҵ��ѧҵ���Ի�ѧģ���Ծ��������棩 ���ͣ���Ϣ������
��8�֣�����ˮ�Ǿ����Դ���⡣��ͼ���ۺ����ú�ˮ�Ʊ���һЩ��Ʒ�����̣�

��1������a �������� ����ʵ��������ɴ��������Ҫ�IJ����������ձ����������� ��
��2����������������ᾧ���������ý��½ᾧ���������� ��
��3�������Ӧ����������� ��
��4����д�������ڡ���������Ӧ�Ļ�ѧ����ʽ��
�� ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ���ݻ������������ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���������������ӵĽṹʾ��ͼ������˵����ȷ����

�� �� �� ��
A������ʾ����ϡ������Ԫ�� B�����ڻ�ѧ��Ӧ�����õ�����
C������ʾ���������� D������ʾ����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com